Расстановка коэффициентов в уравнении онлайн


2) Символы химических элементов следует записывать строго в том виде, в котором они фигурируют в таблице Менделеева. Т.е. первая буква в обозначении символа любого химического элемента должна быть заглавной, а вторая строчной. Например, символ химического элемента марганца следует записать как Mn, но не ни в коем случае как mn и mN;
3) Изредка возникают ситуации, когда формулы реагентов и продуктов записаны абсолютно верно, но коэффициенты все равно не расставляются. Такое может возникать в тех случаях, если коэффициенты в уравнении могут быть расставлены двумя или более способами. Наиболее вероятно возникновение такой проблемы с реакциями окисления органических веществ при которых рвется углеродный скелет. В таком случае попробуйте заменить неизменяемые фрагменты органических молекул на какой-нибудь произвольный символ, например радикал фенил C6H5 можно обозначить как Ph или X. Например, следующее уравнение:
не будет сбалансировано, так как возможна разная расстановка коэффициентов. Однако, введя обозначение C6H5 = Ph, расстановка коэффициентов происходит корректно:
Примечание
В уравнении допускается для разделения формул реагентов от формул продуктов использовать как знак равенства (=), так и стрелку (→), а также случайная запись отдельных букв символов химических элементов не латиницей, а кириллицей в случае их идентичного написания, как, например, символов C, H, O, P.
В случае, если программа оказалась полезной для Вас вы можете поделиться ссылкой на нее с друзьями в социальных сетях (кнопка внизу).
Сумма коэффициентов в уравнении окислительно восстановительной реакции
Сумма,или подбор стехиометрических коэффициентов при написании уравнений окислительно-восстановительных реакций основан на равенстве числа электронов,отдаваемых восстановителем и получаемых окислителем.
Искомая сумма вычисляется в несколько этапов.Рассмотрим на примере реакции лабораторного получения хлора окислением хлороводорода HCl перманганатом калия KMnO4,который при этом восстанавливается до иона Mn+2.
1.Уравнения полуреакций в явном виде(при участии молекул воды):
MnO4[-] + 8H[+] + 5e -> Mn[+2] + 4H2O
2.Необходимо уравнять число электронов в обеих полуреакциях,Первое уравнение надо умножить на 2,второе на 5:
2MnO4[-] + 16H[+] + 10e -> 2Mn[+2] + 8H2O
3.Суммируем уравнения и получаем уравнение в ионном виде:
2MnO4[-] + 16H[+] + 10Cl[-] -> 2Mn[+2] + 8H2O + 5Cl2[0]
В конечном уравнении правая часть должна быть равна левой,включая сумму зарядов ионов(в нашем случае +4,так как 16−10−2=2×2).
Оставить ответ Отменить ответ
Этот сайт использует Akismet для борьбы со спамом. Узнайте, как обрабатываются ваши данные комментариев.
Свежие записи
- Слюна человека содержит фермент который расщепляет
- Фактор,влияющий на смещение химического равновесия.
- Природа связанных химических элементов ионной связи
- Ионное произведение воды водородный показатель
- Какой химический элемент составляет основу алмаза
Рубрики
Образование
- Слюна человека содержит фермент который расщепляет
- Фактор,влияющий на смещение химического равновесия.
- Природа связанных химических элементов ионной связи
- Ионное произведение воды водородный показатель
- Какой химический элемент составляет основу алмаза
- Энтропия что это такое простыми словами
- Основные положения атомно-молекулярной теории
- Особенности ферментативного катализа
- Какой газ называют идеальным.
- Сумма коэффициентов в уравнении окислительно восстановительной реакции
Химические уравнения
Из этой статьи вы узнаете, что такое химические уравнения, зачем они нужны и как их составлять, а также вспомните классификацию химических реакций — все это, конечно, с примерами уравнений.
· Обновлено 29 июля 2023
Химическое уравнение — это условная запись химического превращения с помощью химических формул и математических знаков
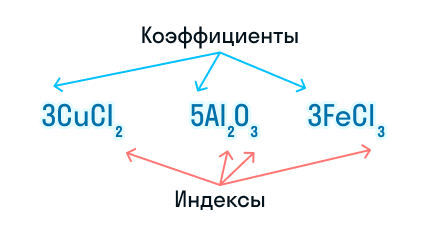
При составлении химических уравнений используют математические знаки «+», «−», «=», а также числа — они выступают в качестве коэффициентов и индексов.
Коэффициенты показывают число частиц (атомов или молекул), а индексы — число атомов, которые входят в состав молекулы.
Химическую реакцию можно изобразить в виде схемы:
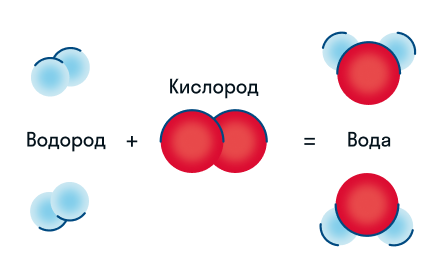
На схеме протекание реакции представлено нагляднее, но сложные химические процессы изобразить таким способом сложно. Поэтому их записывают в виде химического уравнения.
Вещества, которые вступают в реакцию, называют исходными веществами, или реагентами. Вещества, которые образуются в результате, называют продуктами реакции.

Давайте разберем этот пример химического уравнения. Здесь видно, что из двух молекул водорода и одной молекулы кислорода образуются две молекулы воды. Реагенты в данном случае — водород и кислород, продукт реакции — вода.
Новые вещества образуются вследствие перегруппировки исходных атомов. В результате химической реакции атомы химических элементов никуда не исчезают и не возникают новые, их число остается неизменным — это следует из закона сохранения массы веществ.
Закон сохранения массы веществ
Масса веществ, вступивших в реакцию, равна массе веществ, образовавшихся в ходе этой реакции.
Закон сохранения массы веществ лежит в основе химии и используется при составлении уравнений химических реакций.
Алгоритм составления уравнения химической реакции
Рассмотрим, как составлять уравнения химических реакций, на примере взаимодействия магния и кислорода с образованием оксида магния.
- Записываем химические формулы исходных веществ в левой части уравнения. Напоминаем: молекулы H2, N2, O2, F2, Cl2, Br2, I2 двухатомны. Между исходными веществами ставим «+», а затем знак «=».
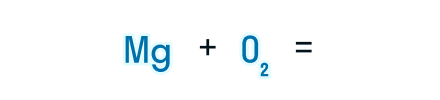
- После знака равенства записываем химическую формулу продукта. Химическую формулу необходимо составить с учетом валентностей химических элементов.
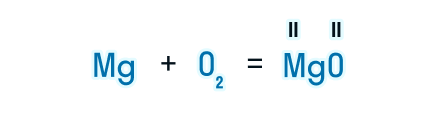
- Согласно закону сохранения массы веществ, число атомов каждого химического элемента до и после реакции должно быть одинаковым. Давайте посмотрим, как расставлять коэффициенты в химических уравнениях, чтобы закон выполнялся. Из составленной химической реакции видно, что количество атомов магния слева и справа от знака равенства одинаково, но атомов кислорода слева два, а справа один. Чтобы уравнять число атомов в химическом уравнении, находим наименьшее общее кратное (НОК), в нашем случае — 2. А затем делим НОК на количество атомов кислорода в реагентах и полученное число записываем в виде коэффициента.
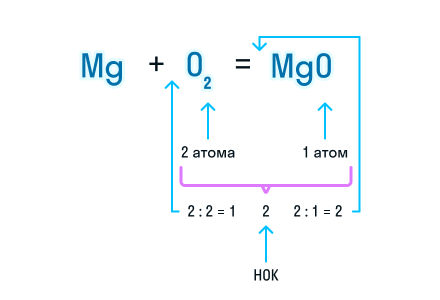
Коэффициент 1 в уравнении химической реакции не указывается, но при подсчете суммы коэффициентов в уравнении его необходимо учитывать.
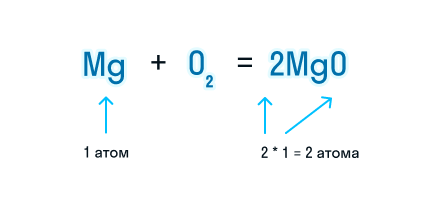
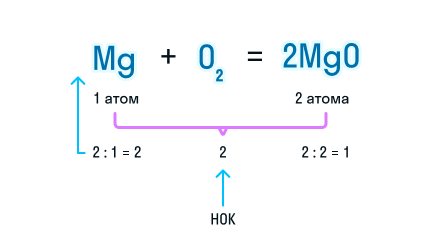
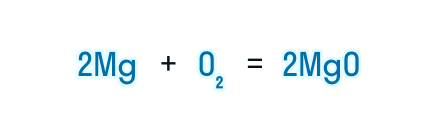
Сумма коэффициентов в этом химическом уравнении равна 5 (2 + 1 + 2 = 5).
Коэффициенты, которые стоят в химическом уравнении перед веществами, указывают на мольное соотношение исходных веществ и продуктов реакции, по которому и производятся расчеты.
Узнай, какие профессии будущего тебе подойдут
10 минут — и ты разберёшься, как стать тем, кем захочешь

Типы химических реакций
Химические реакции можно классифицировать по различным признакам:
- По числу и составу исходных веществ и продуктов реакции.
- По изменению степени окисления.
- По тепловому эффекту.
- По агрегатному состоянию.
- По наличию или отсутствию катализатора.
- По обратимости.
По числу и составу исходных веществ и продуктов реакции
По этому признаку выделяют 4 типа реакций: реакции соединения, реакции разложения, реакции замещения и реакции обмена.
Реакции соединения — это реакции, в результате которых из нескольких более простых веществ образуется одно более сложное.
Например, простые вещества барий и кислород взаимодействуют с образованием сложного вещества оксида бария:
Также к реакциям соединения относится взаимодействие оксида натрия с водой с образованием более сложного вещества гидроксида натрия. Оно более сложное, так как состоит уже из трех атомов химических элементов, в отличие от веществ-реагентов, которые состоят из двух атомов:
Реакции разложения — это реакции, в результате которых из одного более сложного вещества образуется несколько более простых веществ. Является процессом, обратным реакции соединения.
Пример такой реакции — разложение нитрата серебра на несколько более простых веществ: серебро, оксид азота (IV) и кислород.
Что это за стрелочка? ��
Стрелка вверх означает, что получившееся вещество является газом, который покидает место проведения реакции и больше не участвует в ней.
Реакции замещения — это такие реакции, в результате которых атомы простого вещества замещают атомы одного химического элемента в сложном веществе. Также возможно замещение функциональных групп в сложном веществе.
Например, замещение атомов водорода в молекуле соляной кислоты на атомы цинка:
Реакции обмена — это реакции между двумя сложными веществами, в результате которых вещества обмениваются своими составными частями.
Реакции нейтрализации
Реакция щелочи с кислотой называется реакцией нейтрализации и является частным случаем реакции обмена.
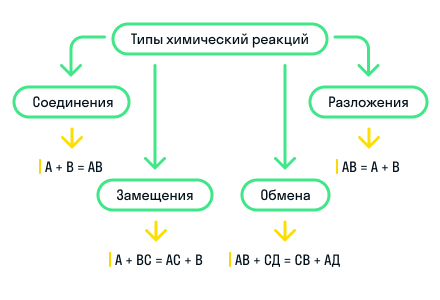
Для наглядности показали все типы химических реакций по этому признаку на схеме:
По изменению степени окисления
По этому признаку выделяют два вида реакций:
- реакции, протекающие без изменения степени окисления;
- окислительно-восстановительные реакции (ОВР) — реакции, протекающие с изменением степени окисления нескольких элементов.
В ОВР всегда участвуют вещество-окислитель и вещество-восстановитель. Другие исходные вещества, принимающие участие в реакции, выступают в качестве среды, в которой протекает эта реакция.
Окислитель — вещество, в состав которого входит ион или атом, который в процессе реакции принимает электроны, тем самым понижая свою степень окисления.
Восстановитель — вещество, в состав которого входит ион или атом, который в процессе реакции отдает электроны, тем самым повышая свою степень окисления.
Из определений можно сделать вывод, что в ходе реакции протекает два процесса: принятие электронов (восстановление) и отдача электронов (окисление). Протекают они одновременно.
По тепловому эффекту
По тепловому эффекту реакции делятся на эндотермические и экзотермические.
Эндотермические реакции протекают с поглощением теплоты (−Q). Буквой Q обозначается количество теплоты.
К таким реакциям относятся практически все реакции разложения. Пример:
Экзотермические реакции протекают с выделением теплоты (+Q).
К таким реакциям относятся практически все реакции соединения. Пример:
По агрегатному состоянию исходных веществ
По этому признаку все реакции разделяют на гомогенные и гетерогенные.
Гомогенные реакции протекают в одной фазе.
К гомогенным реакциям относятся те, исходные вещества которых находятся либо в жидком агрегатном состоянии, либо в газообразном. Например, взаимодействие двух газообразных веществ — водорода и хлора:
Агрегатное состояние указывается в правом нижнем углу: «г» — газообразное, «ж» — жидкое, «тв» — твердое.
Гетерогенные реакции протекают на границе раздела фаз.
Как правило, такие реакции протекают между веществами, которые находятся в разных агрегатных состояниях:
Также к гетерогенным относятся реакции между двумя несмешивающимися жидкостями. Собрали несколько примеров гетерогенных реакций:
Между какими веществами протекает
Тест Коэффициенты в химических уравнениях

Тестирование и выдача сертификатов в соответствии с ФЗ «Об образовании и ФГОС»
Часто задаваемые вопросы
Лицензии и свидетельства
Международный педагогический портал “Солнечный свет” зарегистрирован в Федеральной службе по надзору в сфере связи, информационных технологий и массовых коммуникаций (свидетельство о регистрации СМИ №ЭЛ ФС 77-65391), деятельность портала лицензирована Министерством образования (лицензия на осуществление образовательной деятельности №9757-л).
Какая информация есть в дипломах и свидетельствах?
Наградные документы участников конкурсов, олимпиад и свидетельства, содержат следующие данные и реквизиты: указание на Организатора мероприятия, результат участия, номер, ФИО Участника, должность, наименование представляемой организации, её местонахождение, название мероприятия, название номинации, название конкурсной работы, ФИО руководителя (если есть), дату проведения мероприятия, печать и подпись Организатора. Дипломы, Свидетельства, выдаваемые международным педагогическим порталом «Солнечный свет», являются подтверждающими документами при аттестации согласно Порядку проведения аттестации педагогических работников организаций, осуществляющих образовательную деятельность, утвержденному приказом Минобрнауки РФ от 07.04.2014 г. № 276, и входят в перечень документов и материалов портфолио воспитателя, учителя и других педагогических работников, необходимых для проведения оценки профессиональной деятельности. С помощью них можно также сформировать портфолио достижений дошкольника, школьника.
Ваши мероприятия соответствуют ФЗ «Об образовании» и ФГОС?
Международный педагогический портал «Солнечный свет» проводит международные и всероссийские мероприятия в соответствии с ч. 2 ст. 77 и п. 22 ст. 34 Федерального закона Российской Федерации «Об образовании в Российской Федерации» № 273-ФЗ от 29.12.2012 г. (в ред. от 31.12.2014) направленные на поддержку творческого потенциала педагогических работников и обучающихся. Конкурсы и олимпиады разработаны с учетом требований Федеральных государственных стандартов образования (ФГОС).
В какой срок и как я получу сертификат?
Сразу же после завершения тестирования Вы увидите результат тестирования. Затем в вашем личном кабинете вы сможете ввести данные для формирования сертификата. После оплаты удобным для вас способом мы сразу же предоставим доступ для скачивания сертификата. Также сертификат будет продублирован на вашу электронную почту.