Уполномоченный Представитель изготовителя Европейском Союзе Authorized Representative
Европейский Союз требует, чтобы каждый иностранный производитель, который намеревается продавать свою продукцию в одном из государств-членов ЕС, назначил уполномоченного представителя с физическим адресом в одном из государств-членов.
В связи с усилением ответственности в соответствии с Регламентом 2019/1020 мы обновила свои процессы и системы в соответствии с требованиями.
В отсутствие Соглашения о взаимном признании (MRA) производители вне Сообщества, могут получить доступ на европейский рынок только через европейского представителя.
Рамочные соглашения между странами СНГ и ЕС пока не подписаны.
Работа в качестве Authorised representative, находящегося за пределами ЕС, требует обоснованной юридической, нормативной и технической проверки, которая отвечает наилучшим интересам производства и уполномоченного представителя.
Наша тесная связь и партнерство с ведущими страховщиками ответственности необходимы для того, чтобы предлагать надежные услуги, предлагающие дополнительную ценность помимо «имени на этикетке».
Обеспечиваем готовность вашей технической документации к проверке компетентными европейскими органами, кроме того, он берет на себя ответственность, в случае нарушения законодательства ЕС.
В зависимости от требований, наши услуги выходят далеко за рамки формальных требований официального представителя в Европе.
Authorised representative действует на основании доверенности (договор) производителя продукта, выданной в письменной форме, в которой производитель должен, в частности, указать тип и объем его задач.
Объем доверенности (договора) должен позволять уполномоченному представителю выполнять как минимум следующие задачи:
хранение декларации о соответствии СЕ и технической документации в течение не менее 10 лет с даты размещения продукции на рынке;по обоснованному запросу компетентного органа предоставление этому органу информации и документации, необходимой для демонстрации соответствия данного изделия ЕС декларации о соответствии и другим применимым требованиям, изложенным в соответствующих положениях;по запросу компетентного органа сотрудничество с органом в действиях, предпринятых для устранения рисков, связанных с продукцией, на которую распространяется доверенность.
Сфера действия доверенности может включать в себя составление EC Declaration of conformity ЕС декларации и нанесение маркировки СЕ, но не может включать подготовку технической документации или действий, связанных с производственным процессом, для обеспечения соответствия продукта нормам.
Authorised representative не может модифицировать продукцию по собственной инициативе, чтобы привести его в соответствие с соответствующими положениями. Если он меняет товар или размещает его на рынке под собственной маркой он считается производственником и должен выполнять все обязательства, возложенные на производителя.
Уполномоченным представителем, назначенным производителем, может быть импортер или дистрибьютор в этом случае он также выполняет обязанности импортера или дистрибьютора.
Согласно Директив Нового Подхода производителем является лицом, ответственное за разработку и производство продукта, с намерением разместить его на рынке Европейского союза под своим собственным именем. Производитель также является лицом, которое, например, собирает и или упаковывает продукцию и размещает на нем этикетку с собственным наименованием, он несет ответственность за то, чтобы продукт, который будет размещен на европейском рынке, соответствовал положениям соответствующих директив (-ов), в соответствии с которыми была проведена оценка соответствия основным требованиям.
Задача изготовителя перед размещением продукции на рынке:
обеспечение того, чтобы производственный процесс гарантировал, что продукт соответствует требованиям,разработка технической документации на продукт и оценка соответствия европейским требованиям,составление европейской декларации о соответствии,нанесение маркировки СЕ на продукт,хранение документации в течение 10 лет с даты изготовления последнего изделия (к которому относится документация).
В зависимости от директивы, применимой к продукту, от производственников может потребоваться привлечь уполномоченный орган для контроля и или сертификации продукта или для внедрения системы управления качеством, утвержденной уполномоченным органом.
Директивы нового подхода не требуют, чтобы изготовитель был расположен в Сообществе. Сфера ответственности изготовителя из страны за пределами Европейского сообщества такая же, как и у изготовителей, базирующихся в государстве-члене, поэтому изделия, импортируемые из этих стран, должны соответствовать основным требованиям директив Нового подхода и иметь маркировку CE.
Для облегчения размещения изделия на рынке Сообщества производитель из третьей страны может официально назначить представителя, созданного в Сообществе, который будет действовать от его имени в качестве уполномоченного представителя. Вместо производителя власти государства-члена Сообщества могут связываться с ним по вопросам, связанным с выполнением обязательств производителя в соответствии с директивой Нового подхода.
Как требует Законом о системе оценки, уполномоченным представителем может быть лицо физическое или юридическое, резидент государства-члена Европейского Союза или государства-члена Европейского соглашения о свободной торговле (ЕАСТ), уполномоченный изготовителя в письменной форме действовать от его имени.
Изготовитель должен четко указать объем задач и прав представителя: составление и подписание европейской декларации о соответствии, прикрепление маркировки СЕ и номера уполномоченного органа к продукту, разработка информации, сопровождающей маркировку СЕ (при необходимости), хранение декларации и технической документации в распоряжении национальных властей.
Задачи, возложенные на уполномоченного представителя, носят административный характер, производственник несет ответственность за продукцию и общую ответственность за деятельность, осуществляемую от его имени уполномоченным представителем.
Таким образом, производитель не может делегировать свои обязанности уполномоченному представителю, например, в отношении обеспечения соответствия товара основным требованиям в процессе производства или подготовки технической документации. С другой стороны, уполномоченный представитель не может по собственной инициативе модифицировать продукт, чтобы адаптировать его к требованиям директивы.
Authorised representative может выступать в качестве субподрядчика, например, может участвовать в разработке и или производстве продукта или выступать в качестве импортера продукта, но в этом случае его ответственность вытекает из отдельных соглашений договоренностей с изготовителем.
CE маркировка знак соответствия CE Marking
Маркировка CE является обязательной для ряда продуктов на внутреннем европейском рынке. CE Marking подтверждает соответствие всем директивам и нормам ЕС. Не разрешается наносить знак CE на продукт, на который не распространяется хотя бы одно правовое регулирование CE.
Производитель продукта несет ответственность за CE маркировку. Знак CE должен быть нанесен на продукты, которые подлежат маркировке, до того, как они будут размещены на рынке или введены в эксплуатацию.
Обязательство по маркировке CE распространяется на все продукты, для которых директивы и регламенты предусматривают маркировку CE и которые размещаются на рынке EEA. К продукту могут применяться несколько директив.
Директивы и Регламенты ЕС определяют основные требования безопасности и гигиены для продуктов. Маркировка СЕ подтверждает соответствие требованиям законодательству и показывает, что изделие может размещаться в пределах Европейского экономического пространства стран-членов ЕС и стран-членов ЕАСТ, Исландии, Норвегии и Лихтенштейна.
Не все продукты должны иметь знак СЕ. Запрещается наносить маркировку СЕ на продукты, для которых она не определена.
Продукты, которые предназначены для потребителей или используются потребителями и для которых нет специальных правил, также должны соответствовать требованиям безопасности, к ним применяется директива ЕС «Общая безопасность продукции 2001/95/ЕС». С 2024 года применяется Регламент 2023/988 по общей безопасности продукции.
Размещение на рынке означает любую поставку продукта для распространения, потребления или использования на рынке Союза в ходе коммерческой деятельности, будь то за плату или бесплатно.
У экономических операторов разные обязанности в зависимости от их роли в цепочке поставок. Определенные задачи могут быть выполнены только производителем, так как он знает дизайн и процесс производства продукта в каждой детали. Изготовитель также может назначить уполномоченного представителя для выполнения определенных обязанностей от его имени.
Все экономические операторы должны действовать ответственно и соблюдать все применимые правовые требования при размещении продукта на рынке или при его продаже на рынке.
Производитель это тот, кто производит продукт, или разрабатывает его, или производит, и продает его под своим именем или под собственной торговой маркой. Он отвечает за соблюдение требований безопасности и маркировку СЕ продукции.
У производителя есть следующие задачи:
гарантирует, что продукт был разработан и изготовлен в соответствии с основными требованиями безопасности соответствующих правовых норм ЕС.
проводит оценку соответствия
проводит анализ рисков и оценку рисков, если это необходимо.
готовит техническую документацию.
обеспечивает соответствие в серийном производстве продукции с использованием подходящего процесса.
создает инструкции по применению и необходимую информацию по безопасности на соответствующем языке пользователя. идентифицирует продукт с типом, партией или серийным номером для четкой идентификации. наносит маркировку СЕ и любые другие маркировки на продукт. указывает его имя или торговую марку, а также его почтовый адрес на продукте. издает и подписывает декларацию о соответствии ЕС. хранит техническую документацию и декларацию о соответствии ЕС в течение десяти лет. контролирует свои продукты, доступные на рынке, и при необходимости проводит выборочные проверки. принимает корректирующие меры в случае проблем с продуктом. информирует национальные органы, если продукт опасен. передать всю необходимую информацию и документы национальным органам власти (только по запросу). несет ответственность за дефектные продукты, которые не соответствуют правилам безопасности продуктов ЕС.
Маркировка СЕ должна наноситься производителем (уполномоченным представителем), видимым, разборчивым и нестираемым образом на изделие или его табличку с данными. Если Уполномоченный орган участвовал в этапе контроля производства, его идентификационный номер также должен отображаться.
Директивы и правила ЕС по маркировке CE определяют основные требования по безопасности, которым продукт должен соответствовать.
Проведение процедуры оценки соответствия является необходимым условием для маркировки продукции знаком СЕ. Допустимый процесс указывается в нормах СЕ, применимых к продукту. Некоторые из них предусматривают участие органа, уведомленного государствами-членами ЕС, для проведения необходимых испытаний.
Согласованные европейские нормы помогают доказать, что требования к изделию, перечисленные в правилах гармонизации, соблюдаются. Органы по стандартизации ЕС несут ответственность за подготовку этих технических спецификаций.
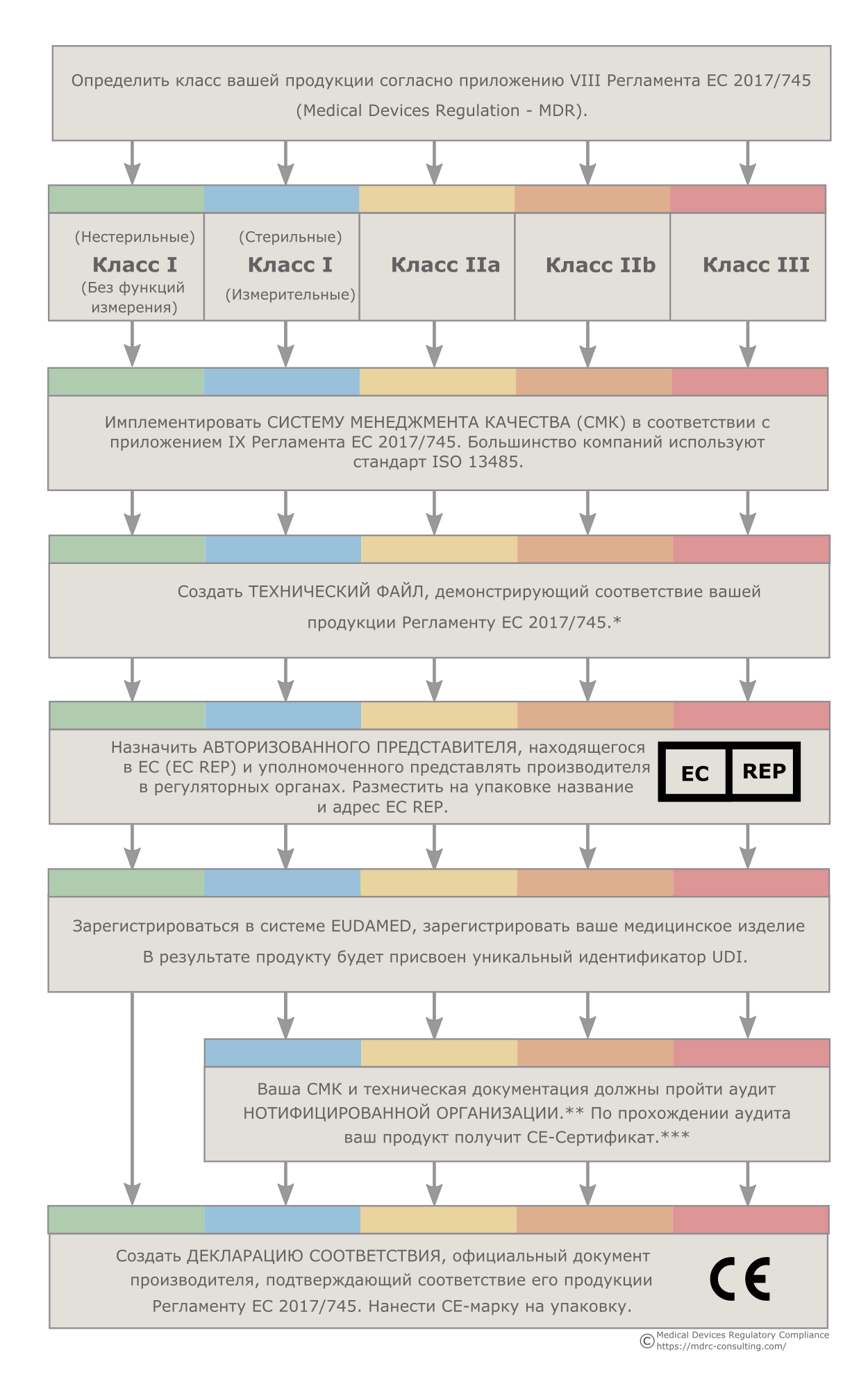
CE-маркировка — регуляторные процессы Европейского Союза для медицинских изделий
*Продукция классов IIb и III с большой вероятностью потребует большого количества клинических данных. В ряде случаев могут использоваться существующие научные данные, но нередко требуется проведение клинических исследований. Клинические исследования, проводимые в ЕС должны быть одобрены Европейскими регуляторными агентствами. Планы и отчеты по клиническим испытаниям помещаются в соответствующий раздел технической документации.
**Нотифицированная Организация — организация, аккредитованная Европейским Союзом на контроль над производителями продукции медицинского назначения.
***CE-Сертификат не выдается продуктам класса I (нестерильным, без функции измерения), поскольку для медицинских изделий данного класса соответствие требованиям Регламента ЕС 2017/745 заявляется производителем в порядке самодекларации.

Скачать брошюру «CE-маркировка для медицинских изделий» в PDF-формате
Как зарегистрировать медицинское изделие в ЕС. Читать статью.
MDRC помогает производителям изделий медицинского назначения достичь соответствия регуляторным требованиям Европейского Союза, зарегистрировать и вывести на европейский рынок их продукцию.
Классификация изделий медицинского назначения
В ЕС определение класса изделий медицинского назначения осуществляется на основе ряда правил, изложенных в приложении VIII Регламента ЕС 2017/745. Поэтому медицинский продукт определенного класса по классификации РФ, США, Китая или другой страны, не входящей в Европейский Союз, в ЕС может относиться к другому классу продукции. Правильное определение класса вашей продукции является критически важным, поскольку от класса будет зависеть то, каким образом будет осуществляться регистрация и вывод на рынок ваших продуктов. Мы поможем вам правильно классифицировать вашу продукцию.
Обучение: CE-маркировка и регуляторная система ЕС для медицинских изделий
Технические файлы и досье разработки
Наличие технического файла является обязательным требованием ЕС, независимо от класса и типа продукта. Досье разработки обязательны для продуктов класса III. Досье разработки отличаются от технических файлов рядом дополнительных требований — в частности необходимостью обширной клинической программы. Мы создали многочисленные технические файлы и досье разработки для целого ряда различных продуктов и готовы помочь вам в создании технической и клинической документации для вашей продукции. Кроме того, мы проводим клиническую оценку продукции, разрабатываем инструкции по применению изделий медицинского назначения и помогаем добиться соответствия ISO 14971.
ISO 13485 и система менеджмента качества (СМК)
У MDRC имеются готовые процедуры и шаблоны документов, которые соответствуют регуляторным требованиям большинства стран и которые могут быть имплементированы в любой компании. Большинство компаний предпочитают использовать стандарт ISO 13485. Мы готовы помочь вам с внедрением СМК. Если у вас уже имеется СМК, мы поможем вам добиться ее соответствия европейским требованиям.
MDR (EU 2017/745) и IVDR (EU 2017/746) требуют наличия у производителя медицинских изделий PRRC (Person Responsible for Regulatory Compliance).
Авторизованное представительство в ЕС (EC REP)
Компании, находящиеся вне Европейского Союза, должны назначить Авторизованного Представителя в ЕС (EC REP), который будет представлять их в регуляторных органах ЕС. Хотя эту роль может выполнять дистрибьютор, наличие независимого Авторизованного Представителя несет в себе большие преимущества, поскольку позволяет менять дистрибьюторов в любое удобное для вас время. Наше германское представительство готово взять на себя роль Авторизованного Представителя для вашей компании.
Аудиты на соответствие требованиям Регламента ЕС 2017/745 и ISO 13485
Производители медицинских изделий классов IIa, IIb и III, а также стерильных продуктов класса I или изделий класса I, предназначенных для измерений, должны ежегодно проходить аудит Нотифицированной Организации. Мы поможем вам подготовиться к аудиту. Помимо этого мы можем провести для ваших работников тренинги по процедурам получения CE-марки, Регламенту ЕС 2017/745, а также внутреннему аудиту.
Взаимодействие с Нотифицированной Организацией
Производители медицинских изделий классов IIa, IIb и III, а также стерильных продуктов класса I или изделий класса I, предназначенных для измерений, взаимодействуют с регуляторными оранами ЕС через Нотифицированные Организации. За поиск и выбор Нотифицированной организации, а также коммуникацию с ней отвечает сам производитель. Мы имеем большой опыт работы с Нотифицированными Организациями из разных стран ЕС и готовы помочь вам выбрать подходящую организацию и наладить взаимодействие с ней.
Оценка и квалификация дистрибьюторов
Согласно Регламенту ЕС дистрибьюторы изделий медицинского назначения в ЕС должны отвечать целому ряду регуляторных требований. Далеко не каждая компания, готовая продавать вашу продукцию, может стать вашим дистрибьютором. В настоящий момент в Европейском Союзе — 27 стран и более 20 официальных языков. Оценка и квалификация дистрибьюторов в таких условиях — непростая задача. Мы поможем вам найти, проанализировать и отобрать подходящих дистрибьюторов.

Получение UDI и регистрация в системе EUDAMED
*Продукция классов IIb и III с большой вероятностью потребует большого количества клинических данных. В ряде случаев могут использоваться существующие научные данные, но нередко требуется проведение клинических исследований. Клинические исследования, проводимые в ЕС должны быть одобрены Европейскими регуляторными агентствами. Планы и отчеты по клиническим испытаниям помещаются в соответствующий раздел технической документации.
**Нотифицированная Организация — организация, аккредитованная Европейским Союзом на контроль над производителями продукции медицинского назначения.
***CE-Сертификат не выдается продуктам класса I (нестерильным, без функции измерения), поскольку для медицинских изделий данного класса соответствие требованиям Регламента ЕС 2017/745 заявляется производителем в порядке самодекларации.
MDRC помогает производителям изделий медицинского назначения достичь соответствия регуляторным требованиям Европейского Союза, зарегистрировать и вывести на европейский рынок их продукцию.
Классификация изделий медицинского назначения
В ЕС определение класса изделий медицинского назначения осуществляется на основе ряда правил, изложенных в приложении VIII Регламента ЕС 2017/745. Поэтому медицинский продукт определенного класса по классификации РФ, США, Китая или другой страны, не входящей в Европейский Союз, в ЕС может относиться к другому классу продукции. Правильное определение класса вашей продукции является критически важным, поскольку от класса будет зависеть то, каким образом будет осуществляться регистрация и вывод на рынок ваших продуктов. Мы поможем вам правильно классифицировать вашу продукцию.
Обучение: CE-маркировка и регуляторная система ЕС для медицинских изделий
Технические файлы и досье разработки
Наличие технического файла является обязательным требованием ЕС, независимо от класса и типа продукта. Досье разработки обязательны для продуктов класса III. Досье разработки отличаются от технических файлов рядом дополнительных требований — в частности необходимостью обширной клинической программы. Мы создали многочисленные технические файлы и досье разработки для целого ряда различных продуктов и готовы помочь вам в создании технической и клинической документации для вашей продукции. Кроме того, мы проводим клиническую оценку продукции, разрабатываем инструкции по применению изделий медицинского назначения и помогаем добиться соответствия ISO 14971.
ISO 13485 и система менеджмента качества (СМК)
У MDRC имеются готовые процедуры и шаблоны документов, которые соответствуют регуляторным требованиям большинства стран и которые могут быть имплементированы в любой компании. Большинство компаний предпочитают использовать стандарт ISO 13485. Мы готовы помочь вам с внедрением СМК. Если у вас уже имеется СМК, мы поможем вам добиться ее соответствия европейским требованиям.
Авторизованное представительство в ЕС (EC REP)
Компании, находящиеся вне Европейского Союза, должны назначить Авторизованного Представителя в ЕС (EC REP), который будет представлять их в регуляторных органах ЕС. Хотя эту роль может выполнять дистрибьютор, наличие независимого Авторизованного Представителя несет в себе большие преимущества, поскольку позволяет менять дистрибьюторов в любое удобное для вас время. Наше германское представительство готово взять на себя роль Авторизованного Представителя для вашей компании.
MDR (EU 2017/745) и IVDR (EU 2017/746) требуют наличия у производителя медицинских изделий PRRC (Person Responsible for Regulatory Compliance).
Аудиты на соответствие требованиям Регламента ЕС 2017/745 и ISO 13485
Производители медицинских изделий классов IIa, IIb и III, а также стерильных продуктов класса I или изделий класса I, предназначенных для измерений, должны ежегодно проходить аудит Нотифицированной Организации. Мы поможем вам подготовиться к аудиту. Помимо этого мы можем провести для ваших работников тренинги по процедурам получения CE-марки, Регламенту ЕС 2017/745, а также внутреннему аудиту.
Взаимодействие с Нотифицированной Организацией
Производители медицинских изделий классов IIa, IIb и III, а также стерильных продуктов класса I или изделий класса I, предназначенных для измерений, взаимодействуют с регуляторными оранами ЕС через Нотифицированные Организации. За поиск и выбор Нотифицированной организации, а также коммуникацию с ней отвечает сам производитель. Мы имеем большой опыт работы с Нотифицированными Организациями из разных стран ЕС и готовы помочь вам выбрать подходящую организацию и наладить взаимодействие с ней.
Оценка и квалификация дистрибьюторов
Согласно Регламенту ЕС дистрибьюторы изделий медицинского назначения в ЕС должны отвечать целому ряду регуляторных требований. Далеко не каждая компания, готовая продавать вашу продукцию, может стать вашим дистрибьютором. В настоящий момент в Европейском Союзе — 27 стран и более 20 официальных языков. Оценка и квалификация дистрибьюторов в таких условиях — непростая задача. Мы поможем вам найти, проанализировать и отобрать подходящих дистрибьюторов.

Получение UDI и регистрация в системе EUDAMED

Скачать брошюру «CE-маркировка для медицинских изделий» в PDF-формате

Как зарегистрировать медицинское изделие в ЕС. Читать статью.
Ec rep что означает маркировка

1.Введение
Маркировка медицинских изделий должна играть важную роль при проектировании, разработке, производстве и остальных этапах жизненного цикла медицинских изделий, в том числе при эксплуатации. К сожалению, практика показывает, что производители либо не уделяют ей и её описанию должного внимания, либо весьма ловко и искусно скрывают свои усилия по этим направлениям. Например, почему в руководстве по эксплуатации нет или очень мало информации о маркировке, её содержании, расположении? Или почему при изучении стадий проектирования или производства медицинского изделия того или иного производителя достаточно часто нет информации о маркировке изделия? Или при изучении файла менеджмента риска медицинского изделия –часто из файла удается только понять, что маркировка на изделии есть, а речи об опасностях и рисках того или иного рода, связанного с маркировкой медицинского изделия, её эксплуатационной пригодностью и «читаемости» ничего не указано?
Конечно же, приведенное выше мнение может показаться чрезмерно пессимистичным. Попробуем разобраться, для чего нужна маркировка, какую информацию о ней требуется или желательно указывать. Причем начнем не с «тяжелой артиллерии» — требований, постановлений, стандартов, а с «конца» — то есть с того, что обычный пользователь изделия, не обязательно медицинского, привык видеть каждый день на маркировках и сопроводительной документации.
2.Идентификация изделий
Можно предположить, что обычный пользователь ничего не знает о требованиях к маркировкам, их содержанию, что их регламентирует, как нужно их описывать. Это в большинстве случаев верно – но в то же время он может наблюдать их повседневной жизни по много раз в день, и таким образом у него складывается свое собственное мнение, что же там должно быть указано. И «поймав» обычного пользователя с предложением пройти опрос, что должно быть на маркировках тех или иных продуктов, можно оказаться достаточно сильно удивленным, когда оный пользователь перескажет Вам чуть ли не большую часть требований стандартов или регламентов, не имея вообще никаких знаний, кроме тех, что такие требования в наше время где-то должны быть описаны. Но эти знания он «приобрел», так как он видел одну и ту же информацию, вернее, один и тот же набор приводимой информации плюс-минус, много тысяч раз.
Можно достаточно долго развивать эту мысль, приводить примеры того, что «клиентоориентированность», «эксплуатационная пригодность» и прочие явные и не явные параметры и свойства важны. Причем весьма вероятен и такой результат изучения определенного продукта пользователем – «у этого производителя это указано / написано / предусмотрено, а у этого – нет, значит первый лучше при прочих равных», то есть можно поговорить и о конкурентной способности изделий. Но вернемся все же к конкретике — информации на маркировках. Приведем ниже предположительное описание информации, полученной от «обычного пользователя» о том, что должно быть на маркировках, с некоторыми комментариями и примерами.
Итак, что же обычный пользователь привык видеть в первую очередь на маркировках изделий? Это наименование продукта – то есть верная и корректная идентификация изделия, скажем так, это аналог ФИО в паспорте в общем смысле этого слова. Иначе, это ответ на вопрос «что находится перед нами?».
Далее — во всех ли случаях указания наименования будет достаточно? Или, скорее, что должно включать в себя наименование? Предположим, что производитель делает несколько моделей под одним наименованием – получается, что наименование должно включать в себя и уточнения, если такие имеются. Большинство производителей, конечно же, так и делает – указывает наименование и модель. Или указывает наименование и номер по каталогу – REF номер (или его аналог). Или все три параметра. Но тут вернемся к предыдущему абзацу и примеру из него – «ФИО в паспорте». Можно было обратить внимание, что это не очень удачный пример – так как в может быть много человек с одним и тем же ФИО в одной стране. И тут-то как раз уже можно выводить достаточно много производителей на «чистую воду» — словосочетание «верная и корректная идентификация изделия» несет в себе смыслы и «полная», и «окончательная» идентификация. Приведем несколько примеров – производитель выпускает свои изделия в разных цветах / разных оформлениях, цвет (оформление) не указан ни в модели, ни в номере по каталогу, ни где-либо еще. Производитель подумает – а зачем? Не будем предполагать, что подумает пользователь о производителе, если он стоит на складе перед двумя одинаковыми коробками без возможности определить, какая коробка содержит изделие нужного ему цвета (оформления).
Можно сказать, что цвет не имеет влияния на функциональные характеристики – не будем заострять внимание на изделиях для детей или для взрослых. Приведем другой пример – производитель поставляет под видом одной модели изделия с разным внутренним устройством – то есть с разными функциональными характеристиками и, более того, более широким-узким назначением. Здесь уже пользователь не во всех случаях по внешнему виду, как для цвета (оформления), сможет понять, какая модификация где. И это очень печально.
Таким образом, подведем итог рассуждениям по поводу наименования, оно же – «верная и корректная идентификация». Пользователь при изучении «полного наименования» изделия, в том числе на маркировке, которое может включать: наименование изделия, модель и номер по каталогу или их аналоги, доп. параметры – не должен задумываться «а правильно ли я все понял», искать какие-либо отличительные признаки, присутствующие на одной модели, но отсутствующие на другой и так далее – информация для идентификации должна быть достаточной и исчерпывающей. Особенно это важно при ситуациях, требующих «экстренных» мер – любая ошибка или задержка в таких случаях может привести к нанесению вреда или чему-либо похуже.
Теперь расширим наш термин «идентификации» другими параметрами — это информация о производителе изделия, его адресе и контактных данных, например, телефоне, адресе электронной почты, сайте – по отдельности и вместе. По сути, это не только вопрос идентификации изделия, так как вполне возможен, пусть даже и с небольшим шансом, случай, когда изделия будут названы полностью одинаково (или производители будут названы одинаково, но располагаться в разных странах), но и указание информации о главном «ответственном» за данное изделие лице. Также для пользователя этот параметр важен, так как чем более известен производитель, там больше доверия он вызывает при прочих равных, тем более качественным считается изделие. Статистически, здесь проблем не бывает – производитель всегда указывает информацию о себе. Проблемы возникают в другом – в актуальности этой информации при изменении её частей – наименовании производителя, его организационно-правовой формы, адреса и т.д. Мы не заостряли внимание на этом раньше – но любая информация, сопровождающая изделие, в том числе на маркировке, должна быть актуальной. И её обновление должно происходить максимально быстро.
Дополнительный параметр, который вытекает из указания информации о производителе – это место производства изделия. Если у производителя несколько производственных площадок или адрес расположения производственной площадки отличается от места расположения офиса производителя, то следует указать и эту информацию, опять же, утрированно, в рамках идентификации и вопроса «кто виноват и где его искать?». Для пользователя этот параметр важен, опять же, по вопросам доверия – чем более «надежной» считается страна расположения производственной площадки, тем большое доверие получает изделие.
Вполне резонно заметить, что если производитель находится за рубежом, то ему необходимо иметь некоторое региональное представительство, как минимум, по законодательным причинам и наличию языковых барьеров, и указывать на маркировке информацию об его Уполномоченном представителе на некоторой территории (некоторой стране, группе стран). Примером данного требования является хорошо известный «EC REP» — Уполномоченный представитель в Европейском сообществе, символ и информацию о котором с 100% вероятностью можно увидеть на маркировках медицинских изделий в ЕС (если он сам не располагается на территории ЕС или его обязанности делегированы).
Укажем ещё один очевидный параметр, который требуется не забыть привести на маркировке – серийный номер или номер партии. Он указывается для идентификации или отслеживания конкретного экземпляра или конкретной партии изделий. Например, для определения, какой конкретно экземпляр изделия требуется отправить на плановое обслуживание, если их несколько на балансе. Или в серийном номере или номере партии достаточно редко, но иногда может кодироваться информация о производственной площадке или дате производства, или модели, или проч. Не забудем и про даты – вот, на что именно пользователь обращает внимание в одну из первых очередей на маркировке и упаковке изделия – дата производства, и, если применимо – дата истечения срока годности (или аналоги) – о них подробней поговорим чуть позже.
Рассмотрим частный случай – изделие представляет собой многоэлементное – чаще в случаях многоразового изделия. Тогда очень важно не забыть промаркировать каждый (при возможности) элемент изделия, и на маркировке элемента указать, как именно он называется. Иначе применение изделия будет затруднено, так как пользователю в общем случае может потребоваться больше времени на изучение, что это за элемент, как его применять, куда его присоединять и т.д.
И еще один частный случай, который скорее относится к дополнительной идентификации производителя, линейки продуктов или конкретного изделия – это товарные знаки. На маркировках часто располагают зарегистрированные соответствующим образом и находящиеся под охраной на определенной территории товарные знаки. Пользователь очень часто наблюдает их на маркировке или упаковке. И, опять же, бренд или товарных знак может вызывать у него разный уровень доверия к изделию. Но достаточно небольшому количеству пользователей будет понятно, почему мы привели именно такую формулировку ранее — «зарегистрированные соответствующим образом и находящиеся под охраной на определенной территории…». Очень часто случается, что производитель забывает, что товарный знак должен быть защищен на территории страны применения его изделия, иначе требуется убрать знаки охраны товарных знаков, информацию о защите товарного знака и проч.
Просуммируем вышеприведенное про информацию на маркировке изделия в рамках идентификации и что на ней требуется обычно указывать:
- Наименование изделия – обязательно для идентификации.
- Модель, номер по каталогу и проч. — обязательно (при наличии) для идентификации.
- Информация о производителе – обязательно для идентификации.
- Производственная площадка – обязательно (при наличии) для идентификации.
- Информация об уполномоченном представителе – обязательно или рекомендуется для идентификации лица, ответственного по определенным активностям на определенной территории обращения изделия.
- Серийный номер или номер партии, даты – обязательно для идентификации.
- Наименование элемента изделия – обязательно для идентификации элемента многоэлементных и, как правило, многоразовых изделий.
- Товарный знак – по желанию при наличии надлежащей регистрации в стране применения.
3.Применение изделия
Перейдем к вопросу – «что обычно располагается на маркировке изделия в целях его надлежащего применения?».
Начнем с того, что на большинстве маркировок располагается указание на применение в соответствии с сопроводительной документацией – то есть на руководство по эксплуатации (инструкцию по применению, руководство пользователя и проч.). Это делается для того, чтобы напомнить пользователю, что изделие допускается применять в соответствии с содержанием сопроводительной документации, и ознакомление с ней перед использованием – обязательно абсолютно для всех изделий (изучение сопроводительной документации и / или описания на упаковке / изделии), и никак иначе. Шутки типа: «инструкцию читают только тогда, когда нечего читать, или уже все безнадежно сломано» — крайне несмешные, особенно для изделий повышенного риска для здоровья, таких, как медицинские изделия. Приводите пользователю требование об обязательном изучении сопроводительной документации везде, где только можно и разумно – пользователь крайне не любит читать инструкции от слова совсем.
Далее, на маркировке изделий также располагают важные запретительные / разрешительные знаки – содержит тот или иной материал – для пользователей с аллергией, использовать повторно нельзя, использовать можно только в помещении, использовать совместно только с таким изделием т.д.
Здесь необходимо заострить внимание на одной проблеме, которая встречается пугающе часто – отсутствие должного описания маркировки и её содержания, расположения. Пользователь, например, может сказать, в некоторых случаях весьма резонно, – «я вижу символ, но не вижу его описания — как я могу понять, что он означает?». Любая ситуация, которая может вызвать вопросы у пользователя – это удар по безопасности и эффективности изделия. Это шанс на возникновение ненадлежащего применения изделия. Практически никогда нет явных причин не указывать описание содержания маркировки.
Еще одним важным параметром, который указывают на маркировке – это даты и временные промежутки – даты изготовления, срок годности, дата окончания срока годности и проч. в различных комбинациях. Для определенных изделий (чаще многоразовых) – это в основном дата изготовления. Для других типов изделий, когда критически важно привести срок годности изделия именно на маркировке (одноразовые стерильные, например), основной акцент приходится на дату окончания срока годности – после её наступления строго запрещено применение изделия. Вариантов указания дат и сроков на маркировке много – только дата изготовления (если в сопроводительной документации указан срок эксплуатации), или дата изготовления и дата окончания срока годности, или дата изготовления и срок годности и др. Главное – точная и простая идентификация даты изготовления и даты окончания возможного применения медицинского изделия.
Также немаловажными параметрами, которые требуются указать на маркировке – это характеристики изделия – их набор зависит от конкретного типа изделия. Например, это могут быть размеры рабочей части – их указывают не «для галочки», а чтобы дать возможность пользователю быстро разобраться, подходит ли данное изделие для применения в конкретном случае. Или электрические параметры – самое простое объяснения их наличия: можно или нельзя подключить в данном месте к сети питания.
Перейдем к очень важному вопросу, который задается производителями очень часто, но вызывает искреннее недоумение – «нужно ли приводить маркировки (и сопроводительную документацию) на языках места обращения изделия?». Обычного пользователя такой вопрос, скорее всего, также сильно удивит. Он спросит: «а как мне применять изделие, если я знаю только родной язык?». Как можно говорить о безопасности и эффективности применения изделия, если пользователь не понимает, что написано на маркировке? Более того, предположим, что мы спросим профессора-лингвиста в каком-нибудь университете: «Скажите, пожалуйста, как Вы думаете, Вы лучше понимаете язык, который изучаете почти всю свою жизнь, по сравнению с обычным носителем языка?». Скорее всего, уважающий себя профессор ответит, что он был бы не столь уверен, что «осилит» «носителя языка» в этом вопросе – то есть подтверждения «полного понимания» написанного на иностранном языке у пользователя, пусть даже и с некоторым приличным уровнем «владения языком», нет. Из чего можно сделать вывод – есть ли требования к указанию маркировок и их содержанию или нет на родном языке в области обращения – не важно, их нужно указывать на языке области обращения (или приводить мультиязычную / несколько моноязычных маркировок).
4.Выводы
Подведем итог наших размышлений – что должно быть приведено и как должно быть приведено на маркировке.
Маркировка должна или может содержать:
- Наименование изделия
- Модель, номер по каталогу и проч.
- Информация о производителе.
- Производственная площадка.
- Информация об уполномоченном представителе.
- Серийный номер или номер партии
- Даты изготовления или даты изготовления и срок окончания применения.
- Наименование элемента изделия.
- Товарный знак.
- Ссылку на «использовать в соответствии с сопроводительной документацией».
- Разрешающие или запрещающие знаки по надлежащему применению изделия.
- Соответствующие данному типу изделий параметры и характеристики.
И, что очень важно, содержать информацию на языке области обращения изделия.