Ptc diagnostic tools что это
Утилита Diagnostic Tools автоматически собирает информацию о приложении и системе и передает ее в PTC. Передача информации осуществляется в соответствии с настройками фильтра на вкладке Фильтры данных (Data Filters) и настройками частоты на вкладке Настройки (Preferences) . В каждой сессии Diagnostic Tools проверяет наличие новых данных перед передачей. Информация автоматически шифруется и передается с использованием методики SSL.
Пользователь приложения Creo может открыть диалоговое окно Diagnostic Tools и просмотреть ожидающие отправки в PTC данные на вкладке Ожидающие решения данные (Pending Data) . Можно нажать кнопку Отправить по электронной почте (Send via-email) , чтобы отправить отчет в формате ASCII, содержащий информацию о приложении Creo и о системе, назначенному инженеру службы технической поддержки PTC и на адрес электронной почты пользователя. И пользователь, и служба технической поддержки PTC могут затем просматривать эти данные одновременно.
Журнал сессии
После завершения сессии установленного приложения Creo создается журнал сессии. Щелкните вкладку Ожидающие решения данные (Pending Data) или Последняя отправка (Last Sent) в диалоговом окне Diagnostic Tools и выберите вкладку приложения, чтобы просмотреть журнал сессии этого приложения. Журнал сессии — это список записей с информацией об определенной сессии.
В журнале сессии содержится информация об идентификаторе сессии, времени начала и завершения сессии, времени бездействия в этой сессии, типе выхода, языковой настройке, использованном сервере лицензий, браузере, версии Java и т.д.
PTC Diagnostic Tools 4
![]()
PTC Diagnostic Tools is a suite of software solutions designed to help industrial manufacturers and service providers optimize the performance of their equipment.
The tools provided by PTC enable real-time monitoring and analysis of operational data, allowing users to quickly identify issues and take proactive measures to prevent downtime, reduce maintenance costs, and increase overall efficiency.
- The suite includes various modules that cater to the specific needs of different industries such as aerospace, automotive, energy, and industrial automation.
- These modules can be integrated with existing software solutions to provide a comprehensive view of the entire supply chain, from design and engineering to production and maintenance.
- The tools also leverage advanced technologies like artificial intelligence and machine learning to enable predictive maintenance and achieve higher levels of operational efficiency.
PTC Diagnostic Tools is suitable for businesses that need to maintain complex equipment or systems that require continuous monitoring. With its easy-to-use interface and robust analytics capabilities, this suite of software solutions helps businesses optimize their operations, reduce downtime, increase profitability, and deliver better value to their customers.
Обзор
PTC Diagnostic Tools это программное обеспечение Shareware в категории (2), разработанная PTC.
Проверяли обновления 346 раз пользователями нашего клиентского приложения UpdateStar в прошлом месяце.
Последняя версия PTC Diagnostic Tools-4, выпущенный на 25.12.2017. Первоначально он был добавлен в нашу базу данных на 30.03.2015.
PTC Diagnostic Tools работает на следующих операционных системах: Windows.
PTC Diagnostic Tools не был оценен нашими пользователями еще.
Написать обзор для PTC Diagnostic Tools!
PTC Diagnostic Tools
How to uninstall PTC Diagnostic Tools from your system
This web page contains detailed information on how to remove PTC Diagnostic Tools for Windows. It was created for Windows by PTC . Open here for more information on PTC. You can see more info about PTC Diagnostic Tools at http://www.ptc.com/support. The application is frequently placed in the C:\Program Files\PTC\DiagnosticTools folder (same installation drive as Windows). The full command line for uninstalling PTC Diagnostic Tools is MsiExec.exe /X. Note that if you will type this command in Start / Run Note you may get a notification for administrator rights. qualityagent.exe is the programs’s main file and it takes circa 58.44 MB (61282800 bytes) on disk.
PTC Diagnostic Tools is composed of the following executables which take 58.44 MB ( 61282800 bytes) on disk:
- qualityagent.exe (58.44 MB)
The current web page applies to PTC Diagnostic Tools version 9.0.3.0 only. You can find below info on other releases of PTC Diagnostic Tools:
- C:\Program Files\PTC\DiagnosticTools
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\Mathcad_Prime_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\phm_translation.xml
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Direct.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Direct_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Direct_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Direct_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Direct_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Direct_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Layout.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Layout_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Layout_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Layout_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Layout_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Layout_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Options_Modeler.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Options_Modeler_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Options_Modeler_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Options_Modeler_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Options_Modeler_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Options_Modeler_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Parametric.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Parametric_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Parametric_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Parametric_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Parametric_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Parametric_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Parametric_Trial.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Parametric_Trial_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Render_Studio.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Schematics.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Simulate.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Simulate_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Simulate_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Simulate_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Simulate_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Creo_Simulate_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\PTC_Windchill_Workgroup_Manager_11_2.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_cn\system_info.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\Mathcad_Prime_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\phm_translation.xml
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Direct.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Direct_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Direct_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Direct_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Direct_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Direct_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Layout.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Layout_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Layout_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Layout_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Layout_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Layout_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Options_Modeler.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Options_Modeler_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Options_Modeler_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Options_Modeler_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Options_Modeler_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Options_Modeler_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Parametric.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Parametric_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Parametric_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Parametric_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Parametric_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Parametric_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Parametric_Trial.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Parametric_Trial_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Render_Studio.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Schematics.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Simulate.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Simulate_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Simulate_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Simulate_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Simulate_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Creo_Simulate_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\PTC_Windchill_Workgroup_Manager_11_2.xslt
- C:\Program Files\PTC\DiagnosticTools\text\chinese_tw\system_info.xslt
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\creo1.sdf
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_chinese_cn_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_chinese_tw_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_french_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_german_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_italian_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_japanese_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_korean_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_portuguese_br_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_russian_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\compiled_resource\phm_default_spanish_resources.dll
- C:\Program Files\PTC\DiagnosticTools\text\french\Mathcad_Prime_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\french\phm_translation.xml
- C:\Program Files\PTC\DiagnosticTools\text\french\PTC_Creo_Direct.xslt
- C:\Program Files\PTC\DiagnosticTools\text\french\PTC_Creo_Direct_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\french\PTC_Creo_Direct_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\french\PTC_Creo_Direct_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\french\PTC_Creo_Direct_Student.xslt
- C:\Program Files\PTC\DiagnosticTools\text\french\PTC_Creo_Direct_Student_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\french\PTC_Creo_Layout.xslt
- C:\Program Files\PTC\DiagnosticTools\text\french\PTC_Creo_Layout_Academic.xslt
- C:\Program Files\PTC\DiagnosticTools\text\french\PTC_Creo_Layout_Academic_old.xslt
- C:\Program Files\PTC\DiagnosticTools\text\french\PTC_Creo_Layout_old.xslt
- HKEY_LOCAL_MACHINE\SOFTWARE\Classes\Installer\Products\410BE024FECA78741AAEE267F1F93440
- HKEY_LOCAL_MACHINE\SOFTWARE\Classes\Installer\Products\410BE024FECA78741AAEE267F1F93440\ProductName
- HKEY_LOCAL_MACHINE\Software\Microsoft\Windows\CurrentVersion\Installer\Folders\C:\Program Files\PTC\DiagnosticTools\
A way to delete PTC Diagnostic Tools from your computer with the help of Advanced Uninstaller PRO
PTC Diagnostic Tools is a program marketed by PTC. Some people want to uninstall it. Sometimes this can be efortful because deleting this by hand requires some knowledge related to Windows internal functioning. The best EASY manner to uninstall PTC Diagnostic Tools is to use Advanced Uninstaller PRO. Here is how to do this:
1. If you don’t have Advanced Uninstaller PRO already installed on your PC, add it. This is good because Advanced Uninstaller PRO is a very efficient uninstaller and all around utility to maximize the performance of your system.
- go to Download Link
- download the program by clicking on the green DOWNLOAD NOW button
- install Advanced Uninstaller PRO
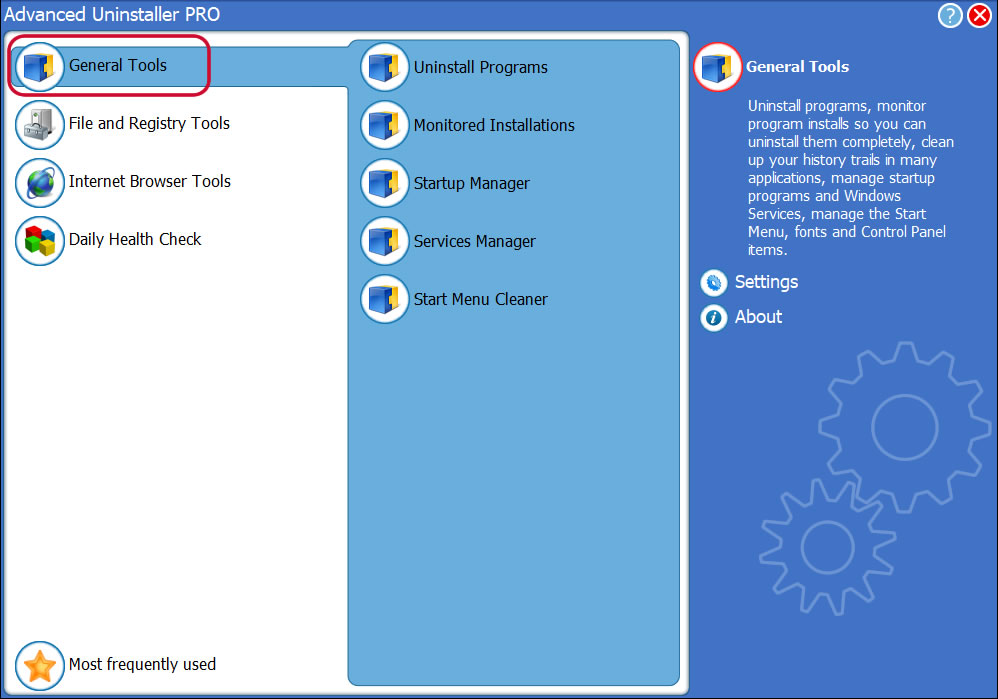
3. Click on the General Tools button
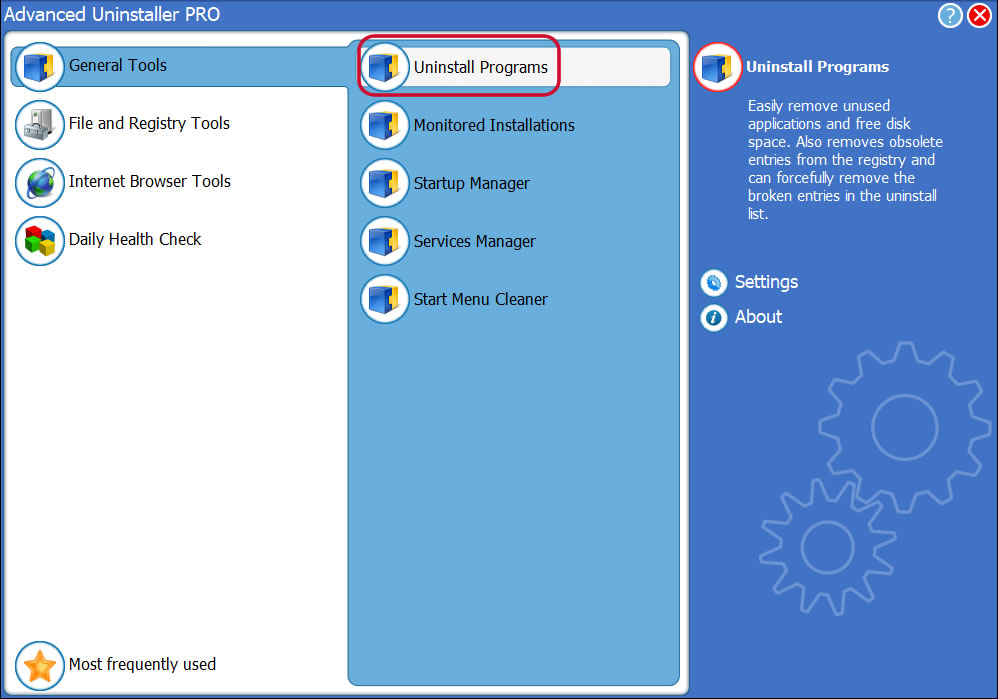
4. Click on the Uninstall Programs button
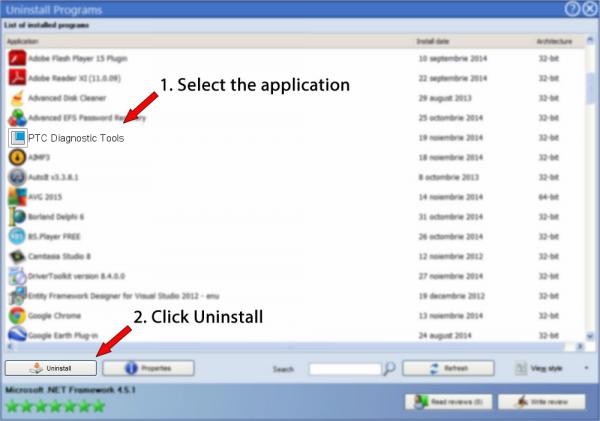
5. A list of the applications installed on your PC will appear
6. Scroll the list of applications until you locate PTC Diagnostic Tools or simply activate the Search feature and type in «PTC Diagnostic Tools». The PTC Diagnostic Tools app will be found automatically. Notice that after you click PTC Diagnostic Tools in the list of applications, the following data regarding the application is made available to you:
- Star rating (in the left lower corner). The star rating explains the opinion other people have regarding PTC Diagnostic Tools, ranging from «Highly recommended» to «Very dangerous».
- Opinions by other people — Click on the Read reviews button.
- Technical information regarding the application you are about to remove, by clicking on the Properties button.
- The web site of the application is: http://www.ptc.com/support
- The uninstall string is: MsiExec.exe /X
7. Press the Uninstall button. A window asking you to confirm will show up. accept the uninstall by clicking the Uninstall button. Advanced Uninstaller PRO will automatically uninstall PTC Diagnostic Tools.
8. After removing PTC Diagnostic Tools, Advanced Uninstaller PRO will offer to run a cleanup. Press Next to start the cleanup. All the items that belong PTC Diagnostic Tools that have been left behind will be found and you will be asked if you want to delete them. By removing PTC Diagnostic Tools using Advanced Uninstaller PRO, you can be sure that no Windows registry items, files or folders are left behind on your system.
Your Windows PC will remain clean, speedy and able to run without errors or problems.
Disclaimer
This page is not a piece of advice to remove PTC Diagnostic Tools by PTC from your computer, nor are we saying that PTC Diagnostic Tools by PTC is not a good application. This text only contains detailed instructions on how to remove PTC Diagnostic Tools in case you want to. Here you can find registry and disk entries that our application Advanced Uninstaller PRO stumbled upon and classified as «leftovers» on other users’ PCs.

2023-03-06 / Written by Dan Armano for Advanced Uninstaller PRO
Молекулярно — генетические маркеры как факторы риска развития рака щитовидной железы
Рак щитовидной железы (ЩЖ) является наиболее распространенной злокачественной опухолью эндокринной системы; за последние десятилетия отмечен рост заболеваемости данной патологией, преимущественно за счет папиллярного рака. Влияние факторов внешней среды, повышение доступности медицинской помощи, в том числе чувствительных диагностических тестов, таких как УЗИ и тонкоигольная аспирационная биопсия (ТАБ), могут повлиять на факт роста данной заболеваемости. Диагностическая ценность пальпации ЩЖ для выявления рака очень низкая, в то время как УЗИ ЩЖ и ТАБ позволяют выявить злокачественные образования в 20% случаев. На сегодняшний день ТАБ узла является наиболее быстрым, точным, экономически доступным и достаточно безопасным методом цитологической диагностики природы узловых образований ЩЖ на дооперационном этапе. С целью унифицирования результатов цитологического исследования в 2009 г. представлена система Bethesda для оценки результатов цитологического исследования ЩЖ. Молекулярно — генетическое тестирование образцов ТАБ может служить дополнительным надежным диагностическим критерием в случае образцов с неопределенным цитологическим диагнозом.
Ключевые слова
Полный текст
ТАБ — тонкоигольная аспирационная биопсия УЗИ — ультразвуковое исследование ЩЖ — щитовидная железа Узловой зоб — собирательное клиническое понятие, объединяющее различные по морфологии объемные образования щитовидной железы (ЩЖ), выявляемые с помощью пальпации и ультразвукового исследования (УЗИ) [1]. Узловые образования щитовидной железы являются общеклинической проблемой. Задача, стоящая перед врачом, заключается в дифференциальной диагностике между злокачественными и доброкачественными образованиями для обеспечения своевременного и соответствующего лечения каждому пациенту и в то же время сведения к минимуму риска неоправданных оперативных вмешательств на ЩЖ по поводу доброкачественных образований. Рак ЩЖ является наиболее распространенной злокачественной опухолью эндокринной системы, за последние десятилетия отмечен рост заболеваемости данной патологией, преимущественно за счет папиллярного рака, на долю которого приходится 90% всех случаев среди мужчин и женщин [2]. Влияние факторов внешней среды, повышение доступности медицинской помощи, в том числе чувствительных диагностических тестов, таких как УЗИ и тонкоигольная аспирационная биопсия (ТАБ), могут повлиять на факт роста данной заболеваемости. Важно отметить, что диагностическая ценность пальпации ЩЖ для выявления рака очень низкая, в то время как УЗИ ЩЖ и ТАБ позволяют выявить злокачественные образования в 20% случаев [3]. Дифференцированный рак ЩЖ представлен эпителиальными опухолями и возникает из фолликулярных (папиллярный, фолликулярный) и парафолликулярных клеток (медуллярный). Большинство видов рака ЩЖ происходят из фолликулярного эпителия, при этом наиболее распространенной является папиллярная карцинома (~80%), за ней следует фолликулярная карцинома (~15%) [4]. Анапластический рак является наиболее редкой, агрессивной формой рака ЩЖ и характеризуется наличием недифференцированных клеток с высоким уровнем митоза. Характерен для старшей возрастной группы и часто возникает в результате накопления мутаций при длительном течении дифференцированных форм [5]. За исключением семейных форм медуллярного рака ЩЖ, в большинстве случаев причиной рака ЩЖ являются спорадические мутации. На сегодняшний день ТАБ узла является наиболее быстрым, точным, экономически доступным и достаточно безопасным методом цитологической диагностики природы узловых образований ЩЖ на дооперационном этапе. С целью унифицирования результатов цитологического исследования в 2009 г. представлена система Bethesda Thyroid Classification для оценки результатов цитологического исследования ЩЖ [6]. Система Bethesda выделяет шесть стандартных диагностических категорий c оценкой риска развития рака ЩЖ в каждой категории. Однако приблизительно в 25% случаев ТАБ не позволяет исключить рак ЩЖ, относя результаты цитологического исследования к одной из трех категорий заключений: атипия неопределенного значения (III категория); фолликулярная неоплазия (IV категория) или подозрение на злокачественную опухоль (V категория) [7]. Такие пациенты подвергаются повторным пункциям и диагностической тиреоидэктомии, что сопряжено не только с экономическими тратами, но и с риском серьезных хирургических осложнений в 2-10% случаев, а большинству из них потребуется назначение пожизненной заместительной терапии левотироксином натрия. Эти данные безусловно подтверждают острую необходимость улучшения предоперационного диагностического обследования пациентов с узловым зобом, особенно с «неопределенным» цитологическим диагнозом. Ряд исследований показал возможность использования молекулярно-генетического исследования для диагностики рака ЩЖ при неопределенных и сомнительных результатах ТАБ [2-6]. С начала 2000-х годов проводятся попытки использовать молекулярно-генетические исследования для улучшения предоперационной диагностики узловых образований щитовидной железы c «неопределенным» цитологическим диагнозом. В течение последующих лет выявление новых генетических аномалий, связанных с раком ЩЖ, позволило провести одновременный анализ большого количества молекулярных изменений и разработать мутационные панели, специально предназначенные для предоперационной диагностики высокодифференцированного рака ЩЖ. Большинство из этих исследований были ретроспективными, где проверялось ограниченное количество генетических изменений, и/или на относительно небольшой группе неопределенных, сомнительных и неинформативных цитологических результатов ТАБ. Последние клинические рекомендации Американской тиреоидологической ассоциации (ATA) 2016 г. рекомендуют исследовать панель из семи мутаций генов (BRAF, NRAS, HRAS, KRAS, RET/PTC1, RET/PTC3, PAX8/PPARγ) в качестве дополнительного метода для стратификации риска малигнизации узлового образования в случае неопределенного заключения цитологического исследования [8]. Исследования последних лет завершились разработкой, с помощью технологии секвенирования следующего поколения (NGS), новых диагностических панелей, таких как AFIRMA и ThyroSeq v3. Панель AFIRMA включает исследование экспрессии мРНК 167 генов, а ThyroSeq v3 — ДНК и РНК 112 генов на различные мутации. Данные панели показали высокую чувствительность и специфичность для диагностики рака у больных с узловыми образованиями ЩЖ, которые имели «неопределенный» цитологический диагноз [9]. На сегодняшний день наиболее изученными мутациями при папиллярном раке ЩЖ являются точечные мутации генов BRAF и RAS, а также перестановки генов RET/PTC. BRAF Точечные мутации гена BRAF выявляются в 40-45% случаев папиллярного рака ЩЖ, это наиболее распространенное молекулярно-генетическое изменение для данной злокачественной опухоли [10]. BRAF представляет собой серин/треонин киназу семейства белков RAF, один из участников сигнального пути Ras-Raf-MAPK. Точечные мутации BRAF обычно включают нуклеотид 1799, что приводит к замене валина на глутамин в остатке 600 (V600E) [11]. Мутация V600E активирует BRAF-киназу, что приводит к продолжительной стимуляции МАРК-пути и, в конечном счете, туморогенезу [12]. Впервые мутация гена BRAF описана для меланомы, а позже и для других раков, в том числе ЩЖ. Мутация BRAF V600E, как правило, представлена в классическом варианте папиллярной карциномы и высококлеточном варианте; редко — в фолликулярной карциноме [11]. Эта мутация встречается также в низкодифференцированных и анапластических карциномах ЩЖ [13]. Определение точечных мутаций BRAF в высокодифференцированных и низкодифференцированных опухолях может свидетельствовать о том, что данная мутация происходит в начальных этапах онкогенеза. Мутация BRAF V600E не идентифицирована в фолликулярных карциномах и доброкачественных образованиях ЩЖ, что может свидетельствовать о том, что данная мутация является специфическим маркером папиллярного рака и связанных с ними типов опухолей [11]. Другие мутации BRAF, в том числе точечная мутация K601E, небольшие вставки в рамке или делеции вокруг кодона 600 и AKAP9/BRAF перестройки встречаются в редких случаях папиллярных карцином (1-2%) [14]. Мутация K601E выявлена в одном случае фолликулярной аденомы [15]. Мутация BRAF V600E также может иметь прогностическое значение в диагностике карцином ЩЖ. Хотя ассоциация BRAF V600E с агрессивным течением и плохим прогнозом при папиллярном раке ЩЖ на сегодняшний день является предметом обсуждения, ряд исследований показал ассоциацию данного генетического маркера с агрессивным течением опухоли, в том числе с экстратиреоидным распространением, поздней стадией на момент постановки диагноза, метастазированием в лимфатические узлы и отдаленными метастазами [16]. BRAF V600E может быть независимым прогностическим фактором неблагоприятного исхода в лечении и рецидива опухоли, даже на первых стадиях заболевания [17], а также независимым фактором риска смертности, связанной с опухолью [18]. В исследовании G.M. Howell и соавт., включившем 219 пациентов с папиллярным раком ЩЖ, показана ассоциация BRAF мутации с рецидивом в группе пациентов пожилого возраста (>65 лет). C.J. O’Neill и соавт. показали больший риск повторных хирургических вмешательств у пациентов с BRAF V600E-позитивными опухолями [19]. В исследовании L. Yip и соавт. BRAF-положительные пациенты чаще нуждались в повторной операции по поводу рецидива/персистенции заболевания по сравнению с BRAF-отрицательными пациентами, в связи с чем высказано предположение, что дооперационное определение мутации BRAF V600E может быть показанием для расширения первоначального плана хирургического лечения, послеоперационной радиойодтерапии в более высокой дозировке, супрессивной терапии, более тщательного наблюдения [20, 21]. Показано прогностическое значение определения точечных мутаций BRAF при T1-папиллярных карциномах, карциномах диаметром ≤2 см, в том числе при папиллярных микрокарциномах. Мутация BRAF V600E ассоциирована с экстратиреоидным распространением и метастазированием в лимфатические узлы при T1-папиллярных карциномах [16], есть сообщения о подобной корреляции при микрокарциномах [22]. В систематическом обзоре и метаанализе 14 публикаций, включивших 2470 пациентов с папиллярным раком ЩЖ из 9 разных стран, показано, что пациенты с BRAF V600E-позитивными опухолями чаще имели ассоциацию с высоким риском рецидивов по сравнению с пациентами без мутаций (24,9% против 12,6%), риск рецидива у пациентов с данной мутацией варьировал от 11 до 40 % (в среднем 26,5%), в то время как у пациентов без мутаций — от 2 до 35% (в среднем 9,5%) [23]. RAS Мутации RAS являются второй наиболее распространенной мутацией, обнаруженной в образцах ТАБ узлов ЩЖ. Семейство человеческих генов RAS включает в себя гены HRAS, KRAS и НRAS. Эти гены кодируют внутриклеточные G-белки, проводящие сигналы от клеточного рецептора тирозинкиназы и G-сопряженных рецепторов по МАРК, PI3K/AKT и другим сигнальным путям. Активирующие точечные мутации в генах RAS распространены в опухолях человека: мутации KRAS в кодонах 12/13 преобладают в большинстве видов рака, в то время как мутации NRAS в кодоне 61 и HRAS в кодоне 61 мутации чаще выявляются в опухолях ЩЖ. При этом мутации генов RAS имеют место при всех типах злокачественных опухолей ЩЖ эпителиального происхождения. Мутации RAS выявляются как в злокачественных, так и в доброкачественных новообразованиях ЩЖ, представлены в 40-50% фолликулярных карцином и 20-40% фолликулярных аденом [24]. Реже мутации RAS выявляются в онкоцитарных вариантах фолликулярных поражений. Эти мутации чаще встречаются при фолликулярном раке и фолликулярном варианте папиллярного рака. Мутации RAS встречаются в 10-20% папиллярных карцином ЩЖ, практически все из которых относятся к фолликулярному варианту [25-27]. Ряд исследований показал высокую частоту мутации RAS в низкодифференцированном и недифференцированном папиллярном раке ЩЖ, по сравнению с высокодифференцированным, однако небольшая выборка пациентов в этих исследованиях не позволяет установить прогностическую роль. Тем не менее мутация гена RAS может предрасполагать, по некоторым данным, к дедифференцировке и агрессивному поведению высокодифференцированного рака, оправдывая хирургическое удаление RAS-положительных фолликулярных аденом [25, 27]. RET/PTC RET/PTC-положительные папиллярные карциномы, как правило, обнаруживаются в более молодом возрасте, имеют классическое папиллярное гистологическое строение и часто метастазируют в лимфатические узлы [26]. RET протоонкоген кодирует клеточную мембрану рецептора тирозинкиназы и хорошо экспрессируется в парафолликулярных или С-клетках ЩЖ. В фолликулярных клетках RET может быть активирован с помощью хромосомной перестройки RET/PTC, что способствует активации MAPK-сигнального пути. Из 11 известных RET/PTC-перестроек наиболее часто в тиреоидных карциномах встречаются RET/PTC1 и RET/ PTC3 [28]. RET/PTC1 встречается в 60-70% всех случаев RET/PTC-положительных карцином, RET/PTC3 присутствует в 20-30% случаев, а на остальные перегруппировки приходится около 5% [29]. Данные о распространенности RET/PTC в опухолях ЩЖ сильно варьируют. Это несоответствие может быть связано с неоднородным распределением RET/PTC-перестроек внутри опухоли, различной чувствительности методик обнаружения, а также разными географическими и этническими группами [30]. RET/PTC1 наиболее часто встречается при классическом гистологическом варианте папиллярного рака ЩЖ, в то время как RET/PTC3-перестройка — при солидном варианте, характеризующемся более агрессивным течением при манифестации [31]. RET/PTC-перестройки часто встречаются при раке ЩЖ после радиационного воздействия (50-80%), а также у детей и лиц молодого возраста (40-70%). В частности, RET/PTC3 часто встречался в случаях детского папиллярного рака ЩЖ после аварии на Чернобыльской АЭС [32]. Перестройки RET/PTC также определялись в фолликулярном варианте папиллярного и фолликулярного рака ЩЖ. Прогностическая роль RET/PTC не до конца изучена, однако опухоли, несущие перестройки RET/PTC, редко прогрессируют до низкодифференцированного и недифференцированного рака ЩЖ. По некоторым данным, обнаружение RET/PTC1 связано с благоприятным поведением папиллярного рака [33]. В отличие от BRAF- и RAS-мутаций, RET/PTC1-перегруппировки связаны с очень низкой вероятностью дедифференцировки в папиллярных карциномах [29], однако RET/PTC3-перегруппировка может предрасполагать к дедифференцировке и более агрессивному течению [34]. Корреляция между RET/PTC-перегруппировкой и прогнозом папиллярного рака ЩЖ требует дальнейшего уточнения. Pax8/PPARy Pax8/PPARy-перегруппировка происходит в результате транслокации t (2; 3) (Q13, P25), что приводит к слиянию гена Pax8 и рецептора гена — активатора пролиферации пероксисом (PPARy) [35]. Эта перегруппировка идентифицируется в 30-40% случаев обычных фолликулярных карцином и реже в онкоцитарных вариантах. Pax8/PPARy-положительные фолликулярные карциномы чаще выявляются в более молодом возрасте, имеют небольшой размер и чаще дают сосудистую инвазию [36, 37]. Pax8/PPARy-перегруппировка также присутствует в небольшом проценте случаев фолликулярного варианта папиллярных карцином [37] и фолликулярных аденом [36]. Pax8/PPARy-положительные фолликулярные аденомы обычно имеют толстую капсулу и иммунофенотипическую характеристику злокачественных новообразований ЩЖ; предполагается, что эти опухоли представляют собой рак in situ или ранее не диагностированную фолликулярную карциному [36]. Pax8/PPARy и RAS точечные мутации являются непересекающимися мутациями в фолликулярных карциномах; это говорит о том, что такие злокачественные опухоли возникают по двум различным молекулярным путям, каждый из которых инициирован либо Pax8/PPARy-перегруппировкой, либо мутацией RAS [36]. В некоторых исследованиях перегруппировка ассоциировалась с мультифокальным течением и сосудистой инвазией, однако нет достаточных данных о прогностической роли Pax8/PPARy при высокодифференцированном раке [38]. Присутствие Pax8/PPARy в фолликулярных опухолях не всегда может указывать на злокачественное поражение, но является основанием для тщательного поиска сосудистой или капсульной инвазии [36]. TERT Впервые мутация TERT описана в 2013 г. при различных вариантах рака ЩЖ [39]. Частота точечных мутаций TERT С228Т и С250Т при дифференцированном раке ЩЖ, по данным разных авторов, достигает 7,5-25%, эта частота выше при низкодифференцированных и недифференцированных карциномах, что может указывать на агрессивное течение опухоли. Исследование T. Liu и соавт. показало отсутствие мутации C228T в доброкачественных опухолях и при медуллярном раке ЩЖ. При этом мутация C228T определялась в 11,7% случаев папиллярных карцином, 11,4% фолликуллярных карцином, в 37,5% случаев низкодифференцированных раков и 42,6% анапластических карцином. Мутация C250T встречается намного реже [39]. В крупном исследовании показано, что сосуществование BRAF V600E- и TERT-мутаций связано с агрессивным течением рака ЩЖ и плохими клиническими исходами папиллярного рака ЩЖ [40]. В американской и китайской когортах пациентов отмечена связь мутации промотора TERT и мутации BRAF V600E с папиллярным раком ЩЖ, кроме того, отмечено частое сосуществование в опухолях обеих мутаций [41, 42]. Аналогичные данные наблюдались в португальской популяции [43]. Однако ряд исследований показал обратную зависимость между мутациями промотора TERT и BRAF V600E, а сосуществование TERT- и BRAFV600E-мутаций не ассоциировалось с повышенной агрессивностью или худшими исходами по сравнению с наличием только мутации TERT [44]. Заключение Молекулярное тестирование на распространенные мутации в образцах ткани ЩЖ, полученных методом ТАБ, может значительно повысить точность цитологической диагностики узловых образований ЩЖ. Однако данная методика требует валидизации на каждой популяции. Наиболее перспективной является возможность использования молекулярно-генетического анализа при цитологическом заключении «атипия неопределенного значения» или фолликулярных изменениях. N.P. Ohori и соавт. оценили наличие BRAF- и RAS-мутаций, RET/PTC- и Pax8/PPARy-перестроек в 117 образцах ТАБ ЩЖ [38] Молекулярный анализ и последующая морфологическая верификация показали, что вероятность рака ЩЖ при атипии неопределенного значения у пациентов с любой из этих мутаций в узле составила 100%, в то время как без какой-либо мутации — лишь 7,6%. Эти данные позволяют предположить, что молекулярно-генетическое тестирование образцов ТАБ может служить дополнительным надежным диагностическим критерием в случае образцов с неопределенным цитологическим диагнозом. На сегодняшний день наиболее распространенные генетические маркеры включают мутацию гена BRAF, точечные мутации RAS и RET/PTC, а также Pax8/PPARy-перегруппировки. Последние рекомендации АTA, опубликованные в 2016 г., показали целесообразность использования молекулярно-генетической диагностики образца, полученного методом ТАБ, с применением панели, состоящей из генов BRAF, NRAS, HRAS, KRAS, RET/PTC1, RET/PTC3, PAX8/PPARγ, как дополнительного метода для стратификации риска малигнизации узлового образования в случае «неопределенной» цитологии [8]. Эти и другие новые молекулярные маркеры, вероятно, улучшат как диагностику злокачественных новообразований ЩЖ, так и тактику интраоперационного и послеоперационного ведения больных с раком ЩЖ. Авторы заявляют об отсутствии конфликта интересов.