Полосатые и линейчатые спектры
Если солнечный свет проходит через стеклянную призму либо дифракционную решетку, тогда появляется хорошо известный всем непрерывный спектр (рисунок 1 ).

Рисунок 1 . Непрерывный спектр

Всякий атомарный разреженный газ издает свет с линейчатым спектром. Кроме того, для всякого химического элемента спектр испускания уникальный, поскольку играет роль «удостоверения личности» данного элемента. Набор линий спектра испускания однозначно говорит, какой химический элемент перед нами.
Так как газ разрежен и атомы слабо взаимодействуют друг с другом, делаем заключение, что свет излучают атомы сами по себе. Поэтому атом характеризуется дискретным, строго определенным набором длин волн испускаемого света. Каждый химический элемент, как мы уже отметили, имеет свой набор.
Спектр поглощения
Атомы испускают свет, переходя из возбужденного состояния в основное. Однако вещество может не только испускать, но и поглощать свет. Атом, поглощий свет, совершает обратный процесс – преобразуется из основного состояния в возбужденное.
Вновь рассмотрим разреженный атомарный газ, но уже в холодном состоянии (то есть при довольно низкой температуре). Свечения газа происходить не будет, поскольку в не нагретом состоянии газ не излучает свет, атомов в возбужденном состоянии оказывается для этого очень мало.
Если сквозь холодный газ проходит свет с непрерывным спектром, тогда появляется картина, как на рисунке 3 .

Рисунок 3 . Линейчатый спектр поглощения
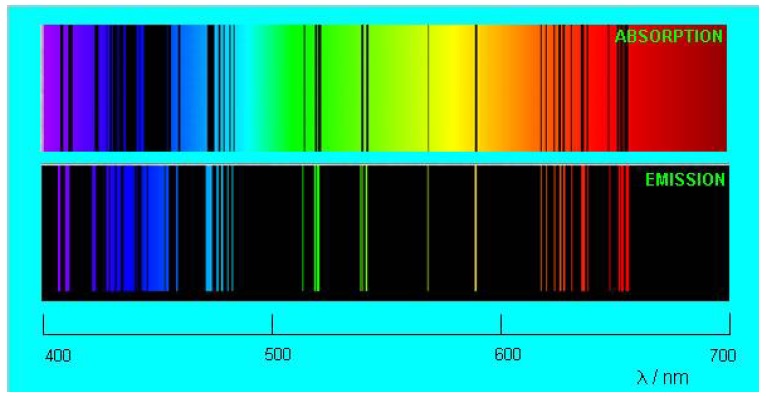
Идея спектрального анализа несложная: спектр излучения анализируемого вещества сопоставляется с эталонными спектрами химических элементов, после чего делается заключение о наличии или отсутствии того или иного химического элемента в этом веществе. При определенных обстоятельствах методом спектрального анализа определяют качественный и количественный состав химического элемента.
В конце наблюдения разных спектров появились новые химические элементы.
Первыми такими элементами были цезий и рубидий. Они были названы по цвету линий своего спектра (в спектре цезия ярко выражены 2 линии небесно-синего цвета, по-латыни называемого “caesius”; рубидий, в свою очередь, испускает 2 характерные линии рубинового цвета).
В 1868 -м г. в спектре солнечного света ученые обнаружены линии, не соответствующие ни одному из открытых на то время химических элементов. Новый элемент назвали гелием (от греческого “гелиос” означает “солнце”). В дальнейшем гелий обнаружили в атмосфере Земли.
Нужно отметить, что спектральный анализ излучения Солнца и звёзд показал: все входящие в их состав элементы имеются и на планете Земля. Таким образом, оказалось, что все объекты нашей Вселенной собраны из одного и того же химического набора.
Лабораторная работа 5
3. Зарисуйте цветными карандашами несколько наблюдаемых вами спектров.
4. Направьте спектроскоп на светящуюся люминесцентную лампу, установленную на демонстрационном столе, и рассмотрите её спектр. Зарисуйте наблюдаемый спектр.

Опишите, чем спектр люминесцентной лампы отличается от спектра лампы накаливания.
Лампа накаливания даёт сплошной спектр, а люминесцентная лампа даёт линейчатый спектр.
5. Вставьте трубку с гелием 1 в держатель 2 прибора для зажигания спектральных трубки подключите прибор к источнику напряжения 3. Зажгите спектральную трубку и рассмотрите в спектроскоп 4 линейчатый спектр излучения гелия. Зарисуйте спектр излучения данного газа и запишите основные цвета в наблюдаемой последовательности.
Фиолетовый, зелёный, оранжевый, красный.

6. Повторите наблюдения со спектральной трубкой, наполненной другим газом. Зарисуйте спектр излучения данного газа и запишите основные цвета в наблюдаемой последовательности.
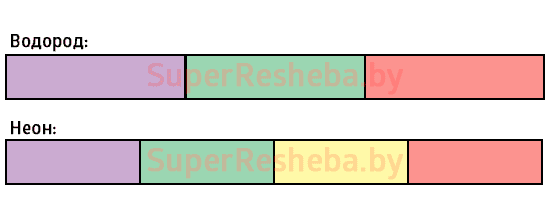
Водород: фиолетовый, зелёный, красный.
Неон: фиолетовый, зелёный, оранжевый, красный.
7. Сравните полученные линейчатые спектры излучения с табличными спектрами излучения соответствующих газов. Сделайте выводы.
Спектры практически не отличаются. Единственное отличие — фиолетовый цвет переливается с голубым.
1. Какие вещества дают сплошной спектр?
Нагретые тела, находящиеся в твёрдом и жидком состоянии, газы при высоком давлении и плазма.
2. Какие вещества дают линейчатый спектр?
Те вещества, у которых слабое взаимодействие между молекулами, например достаточно разряжённые газы. Также линейчатый спектр дают вещества в газообразном атомном состоянии.
3. Объясните, почему отличаются линейчатые спектры различных газов.
При нагревании часть молекул газа распадаются на атомы, излучаются кванты с различными значениями энергии, от чего и зависит цвет.
4. Почему отверстие коллиматора спектроскопа имеет форму узкой щели? Изменится ли вид наблюдаемого спектра, если отверстие сделать в форме треугольника?
Отверстие имеет форму узкой щели для создания картинки. Если отверстие сделать треугольным, то линейчатый спектр станет треугольным и размытым.
Выводы: сплошные спектры дают тела в твердом или жидком состоянии, а также сильносжатые газы. Линейчатые спектры дают вещества в атомарном газообразном состоянии.
Обьясните, почему отличаются линейчатые спектры различных газов?
Потому что такие спектры наблюдаются в тех условиях, когда часть молекул газа распадается на атомы. Электроны в атомах, в свою очередь, способны переходить из основного состояния в возбужденное. Возбуждённое состояние является, как правило, короткоживущим, поэтому далее происходит «ступеньчатое» возвращение назад, снова в основное состояние. При этом электрон «прыгает» с одной орбитали на другую, подчиняясь определённым законам (прежде всего, правилам отбора). Этот процесс (в полном согласии с законом сохранения энергии) сопровождается излучением квантов с различными значениями энергии. Но орбитальная структура для каждого атома — своя, а значит и энергии излучаемых квантов, которые определяют линейчатый спектр, будут существенно зависеть от конкретного атома.
Остальные ответы
Молекулы разных газов при облучении светом одной частоты выдают излучения другой частоты (частот) , характерных для данного газа. На этом принципе работает спектрограф, сопоставляя каждой частоте излучения газ, сверяясь по заранее подготовленным значениям.
Частота излучаемого света зависит от электронного строения атома, при переходе электрона с одной орбиты на орбиту с меньшей потенциальной энергией излучается фотон с энергией h*ню, где ню — частота излучения, h — постоянная Планка.
разный заряд атомов
Похожие вопросы
Чем отличаются линейчатые спектры различных газов
Физика
Электродинамика
Магнитное поле
Механические колебания
Электромагнитные колебания
Механические волны
Электромагнитные волны
Оптика
Геометрическая оптика
Задачи на сферическое зеркало
Линза
Волновая оптика
Основы теории относительности
Основы квантовой физики
Излучения и спектры
Световые кванты
Атомная физика
Ядерная физика
Физика элементарных частиц
Открытие позитрона. Античастицы
Современная физическая картина мира
Современная физическая картина мира
Строение Вселенной
Строение Вселенной
Звёзды и источники их энергии. Современные представления о происхождении и эволюции Солнца и звёзд
Наша галактика и другие галактики
Пространственные масштабы наблюдаемой Вселенной
Применимость законов физики для объяснения природы космических объектов
«Красное смещение» в спектрах галактик
Современные взгляды на строение и эволюцию Вселенной
Наблюдение солнечных пятен, звёздных скоплений, туманностей и галактик
Медиаматериалы