Оценка растворимости солей щелочных металлов Текст научной статьи по специальности «Химические науки»
РАСЧЕТ РАСТВОРИМОСТИ / СВОБОДНАЯ ЭНЕРГИЯ ГИББСА ПРОЦЕССА РАСТВОРЕНИЯ / ЭНЕРГИИ ОБРАЗОВАНИЯ КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ / ЭНЕРГИЯ ГИДРАТАЦИИ / CALCULATION OF SOLUBILITY / FREE ENERGY OF GIBBS OF DISSOLUTION PROCESS / ENERGY OF A CRYSTAL LATTICE FORMATION / HYDRATION ENERGY
Аннотация научной статьи по химическим наукам, автор научной работы — Артамонова И. В., Леснова Л. А., Русакова С. М., Годунов Е. Б.
Проведен расчет растворимости солей щелочных металлов с использованием двух подходов: термодинамического (энергетического) и по значениям величин заряда и радиуса иона. Дана оценка растворимости солей и гидроксидов элементов 1А подгруппы периодической системы химических элементов.
i Надоели баннеры? Вы всегда можете отключить рекламу.
Похожие темы научных работ по химическим наукам , автор научной работы — Артамонова И. В., Леснова Л. А., Русакова С. М., Годунов Е. Б.
Термодинамические и кинетические основы аммиачно-аммонийного извлечения соединений цинка и меди из техногенных отходов
Термодинамический анализ реакции образования силиката кадмия в водных растворах
Растворимость и соотношение масс ионов у солей, кислот и оснований
растворимость галоидов щелочноземельных металлов
Термодинамический расчет растворимости фосфатов редкоземельных металлов при различных температурах и концентрациях ортофосфорной кислоты
i Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
i Надоели баннеры? Вы всегда можете отключить рекламу.
Evaluation of alkali metals salts solubility
Calculation of alkali metals salts solubility is made using two approaches: thermodynamic (or power) and on values of charge and ionic radius sizes. The estimation of salts and oxyhydroxides solubility for elements of 1А subgroups of periodic table is given.
Текст научной работы на тему «Оценка растворимости солей щелочных металлов»
Серия 3. ЕСТЕСТВЕННЫЕ НАУКИ
Оценка растворимости солей щелочных металлов
к.х.н. доц. Артамонова И.В., к.т.н. доц. Леснова Л. А., к.х.н. Русакова С.М., Годунов Е.Б.
Университет машиностроения 8-926-664-30-40, dolgaleva_inna@ma.il. ги
Аннотация. Проведен расчет растворимости солей щелочных металлов с использованием двух подходов: термодинамического (энергетического) и по значениям величин заряда и радиуса иона. Дана оценка растворимости солей и гидро-ксидов элементов 1А подгруппы периодической системы химических элементов.
Ключевые слова: расчет растворимости, Свободная энергия Гиббса процесса растворения, энергия образования кристаллической решетки, энергия гидратации.
Работа выполнена при финансовой поддержке государственной программы «Научные и научно-педагогические кадры инновационной России на 2009-2013 годы» (контракты №14.740.11.1095, 16.740.11.0679) и аналитической ведомственной целевой программы (шифр заявки № 3.5258.2011).
Понятие о растворимости различных веществ можно использовать для предсказания направленности (возможности) протекания химических реакций. В таблице растворимости собраны экспериментальные данные по хорошо-, мало- и нерастворимым веществам. Известно, что абсолютно нерастворимых веществ нет. Растворимость (Б) выражается в моль/1000г Н20 или моль/л, г/100мл и проч., но можно использовать энергетические представления, например, Свободная энергия Гиббса процесса растворения (АО, кДж / моль), тепловой эффект процесса (АЯ). Процесс растворения идет самопроизвольно (АС < 0), и
раствор остается ненасыщенным, т.е. в раствор еще может переходить некоторое количество вещества. Когда АО = 0 система находится в равновесии, раствор становится насыщенным, в таком растворе неопределенно долго могут существовать без каких-либо изменений раствор и избыток растворяемого вещества. Для решения прикладных задач необходимо уметь провести оценку растворимости различных веществ.
Цель работы — провести анализ растворимости элементов 1А подгруппы периодической системы химических элементов с использованием термодинамического (энергетического) подхода и с учетом величин заряда и радиуса иона.
Растворимость любого вещества (Б) равна его концентрации в насыщенном растворе. Термодинамические расчеты позволяют рассчитать величины растворимости Б и произведение растворимости (ПР) и установить между ними связь[1-4].
Для примера рассчитаем растворимость двух солей ЫЕ и CsF , используя термодинамический подход (энергетический). Если взять соль и поместить ее в водный раствор, то между осадком и насыщенным раствором устанавливается равновесие вида:
Для соли (1) можно написать произведение
Если концентрацию ионов серебра обозначить б, то концентрация фторид-ионов тоже будет равна б. Отсюда
ПР= [ П+ ] • [ Г — ] =Б2, Б= л/ПР . Правильнее использовать понятие активная концентрация: аи+ = у^П,
где у — коэффициент активности, для упрощения расчетов принимают равным 0.
В случае если в справочниках отсутствуют значения ПР, то его можно рассчитать с использованием Стандартной энергии Гиббса. Как известно, ПР и растворимость малорастворимого электролита можно связать с энергией Гиббса следующим уравнением [1]:
-АО0 = 2,3 • ЯТ ПР = 2 • 2,3ЯТ £ . (3)
Для любых реакций изменение Свободной энергии Гиббса равно разности из сумм энергий образования конечных продуктов и свободной энергии образования исходных веществ (АО0) . Здесь (АО0) — изменение свободной энергии Гиббса образования любого
вещества из простых веществ ( ^ ) при стандартных условиях (0) .
По уравнению Гиббса рассчитаем АО реакции (1):
А°( _ )=Д Оп +) + А О .¡-А Оиг . (4)
Из справочных данных [4] известно, что:
А = -588 кДж/моль АуОсГ = -528 кДж/моль
А = -293 кДж/моль А ^Ос^ = -292 кДж/моль
А О _ = -280 кДж/моль.
Подставляя соответствующие величины в уравнение (4), получим: АО(расте) = (- 293 — 280)- (- 588) = 15 кДж/моль.
2,3ЯТ = (2,3 • 8,314 • 298) = 5,71 кДж/моль
^ ПР = -АОраств /2,3ЯТ = -15/5,71 = -2,63 ,
Таким образом, зная величину АО0, имеем 1§ £ = -1,315. Отсюда £ш = 0,05 моль/л.
Аналогично можно рассчитать растворимость для хорошо растворимой соли СбГ. Проведя соответствующие расчеты, получим:
АО0раств (СбГ) = — 44 кДж/моль, £ (СбГ) = 7,16-103 моль/л.
Растворимость и энергия растворения (^ / АОраств) солей для ионов щелочных металлов представлены в таблице 1.
Растворимость (8, моль/л) и энергия растворения ( АОраств, кДж/моль)солей щелочных
анион ы+ Ыа+ К+ КЪ+ С5 +
F» 0,05/+15 0,37/5 125,89/-24 3,89-103/-41 7,16-103/-44
СГ 3,20-103/-40 6Д7/-9 2,151-5 4Д2/-7 5,01/-8
Вг~ 1,20-105/-58 30,90/-17 4Д2/-7 4Д2/-7 30,907-17
Г 1,20-105/-58 231,74/-27 7,50/-10 4Д2/-7 1,23/-1
Из анализа данных таблицы 1 следует, что плохо растворимыми солями являются ЫГ, №Г и Сб1. Для солей лития растворимость увеличивается от фторида до иодида. Для солей
цезия растворимость наблюдается обратная зависимость, то есть в направлении от фторида к иодиду растворимость падает. Полученные результаты хорошо согласуются с опытными значениями.
Теперь с помощью энергетических представлений попытаемся ответить на вопрос: почему одни соли хорошо растворимы в воде, а другие — нет?
Как известно, при растворении твердых веществ происходит два процесса: разрушение кристаллической решетки и образование сольватов (гидратов). Эту идею можно выразить формулой:
-2 • 2,3ЯГ 5 = АОраств-АОкрреш. (5)
От соотношения между энергией, необходимой на разрушение кристаллической решетки ( АОкр реш ), и энергией гидратации ( АОгидр) будет зависеть растворимость твердых веществ.
Из уравнения (5) следует, что если энергия гидратации больше, чем энергия кристаллической решетки, то соль хорошо растворима в воде (например, ЬП, ^ CsF ), если энергия кристаллической решетки больше, чем энергия гидратации, то соль плохо растворима в воде (например, ЬiF, ^ Ся1). Соотношение между энергией гидратации и энергией кристаллической решетки можно продемонстрировать графически с помощью энергетического цикла (например, Борна-Габера, где процесс растворения разбит на стадии: разрушение кристаллической решетки и образование гидратов) на примере ЫР (рисунок 1).
Рисунок 1. Энергетический цикл Борна-Габера на примере Е1Е: АОкрреш — та энергия, которая необходима для превращения твердого вещества в ионы в газовой фазе; АОраств — та энергия, которая необходима для превращения твердого вещества в ноны в жидкой фазе; АОгидр — та энергия, которая необходима для перевода ионов из газообразного
состояния в ионы в жидком состоянии
На рисунке 2 показано изменение энергии кристаллической решетки и энергии гидратации фторидов элементов 1-ой группы главной подгруппы.
Как следует из приведенных данных, растворимость фторида лития (ЬiF ) мала, т.к. А^кр.реш > АОгвдр, фторид цезия (№ ) хорошо pacтвopим, т.к. АОкрреш < АОгидр.
Существует еще один более современный подход при оценке растворимости веществ, связанный с величинами заряда и радиусами ионов. Этот подход базируется на следующих уравнениях, выражающих зависимость энергии образования кристаллической решетки и гидратации от заряда и радиуса катиона и аниона.
Энергия кристаллической решетки описывается уравнением Капустинского [2, 3, 5]:
где т- константа.
Как видно из рисунка 2, энергия кристаллической решетки уменьшается с увеличением
радиуса катиона, если радиус аниона постоянен, и, наоборот, при постоянном радиусе катиона с увеличением радиуса аниона.
Рисунок 2. Изменение энергии кристаллической решетки и энергии гидратации фторидов элементов первой группы главной подгруппы (1А)
С уменьшением заряда ионов энергия кристаллической решетки также уменьшается.
Энергия гидратации как катиона, так и аниона можно описать уравнением Борна [2, 3, 5]:
Из уравнения Борна следует, что чем выше радиус, тем ниже AG.
Из совместного решения уравнений Капустинского и Борна следует, что если радиусы катиона и аниона одинаковы, то AGKppem становится больше, чем энергия гидратации. В этом
случае AGKppem » AG и соль плохо растворима (например, в случае LiF ). Если радиусы
катиона и аниона резко отличаются, то согласно уравнениям (6)-(7) AG » AGKppemn соль
хорошо растворима (например, CsF ).
На основе вышеизложенных принципов можно рассчитать и объяснить растворимость веществ, что имеет большой интерес для регулирования процессов растворения. Если перед нами стоит цель осадить какой-либо катион, то мы должны подобрать такой анион, который имел бы одинаковый по размеру с ним радиус. Если мы хотим повысить содержание в растворе какого-нибудь катиона или аниона, то нам следует внести в решетку катион или анион с различными по размеру радиусами.
1. Кумок В.Н., Кулешова О.М., Карабин Л.А. Произведение растворимости. Новосибирск: Наука, 1983г., 267с.
2. Хьюи Дж. Неорганическая химия. Строение вещества и реакционная способность. Москва: Химия, 1987г., 696с.
3. Джонсон Т. Термодинамические спектры неорганической химии. Москва: Мир, 1985, 328с.
4. Лидин P.A., Андреева Л.Л., Молочко В.А. Справочник по неорганической химии. Константы неорганических веществ. М.: Химия, 1987г., 320с.
5. Артамонова И.В., Пришлецова Т.В., Горичев И.Г. Оценка растворимости хлоридов металлов //Актуальные проблемы качества образования и пути их решения в контексте европейских и мировых тенденций. Сборник материалов 10 межвузовской научно-методической конференции Москва: МГУП, 2008г., с. 162-166.
Если элемента нет в таблице растворимости это значит что он точно растворимый да? просто написано что литий очень хорошо
Там есть литий. Только хз сколько модератор ссылку будет проверять. Вообще, наберите в Яндексе «таблица растворимости», и все.
А пользоваться таблицей просто. Таблица показывает растворимость СОЛЕЙ (и гидроксидов) .
Соль состоит из катиона (в таблице это катионы металлов, катион водорода и катион аммония) и аниона (кислотный остаток или гидроксид-ион) . Находите строчку с нужным кислотным остатком и столбец с нужным катионом. На пересечении будет значок.
Легенда обычно такая: Р- растворим, М- малорастворим, Н- нерастворим, —в водной среде разлагается, ?-нет достоверных сведений о существовании соединения.
Р- растворим, М- малорастворим, Н- нерастворим, —в водной среде разлагается, ?-нет достоверных сведений о существовании соединения.
Малорастворим — это значит растворим по сравнению с Н, но нерастворим по сравнению с Р
Иногда бывают продвинутые таблицы, с цифрами, но, я думаю, Вам они не нужны
ЗЫ: элемент сам по себе обычно нерастворим в воде. Либо с ней реагирует, либо нет. Растворимость в ключе данной таблицы относится к солям! Катионов многих металлов в таблице нет не потому, что все их соли хороо растворимы, а потому, что эта информация школьникам не нужна
Остальные ответы
Литий просто горит в воде. Какая растворимость?!
если все элементы и кислотные остатки собрать в таблицу растворимости, то получится очень большая таблица, потому что существует очень много кислот, не только тривиальных, но и новых органических, и искусственно синтезированных. А, вообще, понимать её очень легко. это как таблича умножения, нашел пересечения аниона и катиона и смотришь на ссылку внизу таблицы: Р- растворим, М- малорастворим, Н- нерастворим, —в водной среде разлагается, ?-нет достоверных сведений о существовании соединения.
Форум химиков
Собираюсь выпускать в тираж. Может, какие вопросы/уточнения/ошибки заметите — пишите.
2^74207281-1 is prime!
SkydiVAR Сообщения: 9502 Зарегистрирован: Пн янв 19, 2009 12:51 am Контактная информация:
Re: Обновил таблицу растворимости
Сообщение SkydiVAR » Пн авг 25, 2014 2:49 pm
Вопросы «навскидку»:
У кислот три ступени градации, у оснований только две. Где основания «средней силы»?
Са(ОН)2 попал в щелочи, невзирая на слабую растворимость.
Гидроксид аммония — не щелочь?
Следует ли среди слабых оснований выделить амфотерные?
Спорить не буду. Просто это те вопросы, которые возникли сразу. Возможно, есть обоснование именно такого представления с точки зрения преподавания в средней школе?
Меч-кладенец — оружие пофигистов.
Droog_Andrey Сообщения: 2664 Зарегистрирован: Сб сен 29, 2007 8:29 pm Контактная информация:
Re: Обновил таблицу растворимости
Сообщение Droog_Andrey » Пн авг 25, 2014 3:51 pm
Разумеется, гидроксид кальция — щёлочь, а гидроксид аммония — нет. Сила основания не связана с его растворимостью.
Амфотерные гидроксиды можно было бы выделить, начиная с гидроксида меди. Я думал об этом. Но тогда туда попадёт двухвалентная ртуть, амфотерность гидроксида которой под вопросом. Впрочем, можно сослаться на существование меркуратов, как это делает Третьяков.
P.S. Сделал-таки три степени градации для оснований Картинка по ссылке в первом сообщении обновилась.
2^74207281-1 is prime!
maze Сообщения: 1141 Зарегистрирован: Чт фев 09, 2012 3:41 pm
Re: Обновил таблицу растворимости
Сообщение maze » Пн авг 25, 2014 7:17 pm
Полезная для школьников табличка. Мне такой не хватало, приходилось самой себе рисовать.
Вот ещё сама себе я приписывала цвета нерастворимых соединений. Может, мелким шрифтом или с сокращениями добавить?
И нерастворимые соединения в зелёной гамме как-то вводят в ступор. Может, немного красного? Хотя это уже моя фантазия и привычка. Если вписать цвета осадков, то и без того всё будет ясно.

[ Post made via Android ]
Droog_Andrey Сообщения: 2664 Зарегистрирован: Сб сен 29, 2007 8:29 pm Контактная информация:
Re: Обновил таблицу растворимости
Сообщение Droog_Andrey » Пн авг 25, 2014 8:11 pm
Будет слишком пестро, да и цвета часто зависят от условий получения. Общий дизайн в бирюзовых тонах — поэтому такая гамма.
По содержанию может какие замечания будут? Обычно в таблицах растворимости тонны ошибок, я все данные старался брать из серьёзных источников и выверять.
2^74207281-1 is prime!
maks Сообщения: 14895 Зарегистрирован: Вс апр 19, 2009 3:32 pm
Re: Обновил таблицу растворимости
Сообщение maks » Пн авг 25, 2014 8:19 pm
аммоний карбонат , и другие слабокислотные все же совсем неустойчивы, может другим цветом и написать гидролиз мол
а так отлично , школьникам удобно и дидактически хорошо выстроено
он химик, он ботаник-князь Федор , мой племянник
Droog_Andrey Сообщения: 2664 Зарегистрирован: Сб сен 29, 2007 8:29 pm Контактная информация:
Re: Обновил таблицу растворимости
Сообщение Droog_Andrey » Пн авг 25, 2014 8:27 pm
Фосфат, карбонат и сульфид аммония устойчивы в виде растворов, хоть и значительно гидролизованы там. Мы не можем допускать произвола в том, при какой степени гидролиза считать вещества неустойчивыми в таком случае, тем более что она зависит от концентрации.
Я думал добавить звёздочку «разлагается при выделении из раствора». Она бы легла как на эти соли, так и на гидроксид аммония, сернистую, хромовую и угольную кислоты, а также на гексафторкремниевую кислоту и её соли с Hg(II), Al(III), Fe(III) и Cr(III).
2^74207281-1 is prime!
chaus Сообщения: 3135 Зарегистрирован: Вт дек 24, 2013 2:37 pm
Re: Обновил таблицу растворимости
Сообщение chaus » Пн авг 25, 2014 8:31 pm
Из сильных кислот почему-то не обнаружил хлорной. Хотя она часто применяется в лабораторной практике.
When you open your heart to patriotism, there is no room for prejudice.
SkydiVAR Сообщения: 9502 Зарегистрирован: Пн янв 19, 2009 12:51 am Контактная информация:
Re: Обновил таблицу растворимости
Сообщение SkydiVAR » Пн авг 25, 2014 8:35 pm
Droog_Andrey писал(а): Я думал добавить звёздочку «разлагается при выделении из раствора»
Как по мне — «плюсадин», как минимум.
Меч-кладенец — оружие пофигистов.
Droog_Andrey Сообщения: 2664 Зарегистрирован: Сб сен 29, 2007 8:29 pm Контактная информация:
Re: Обновил таблицу растворимости
Сообщение Droog_Andrey » Пн авг 25, 2014 8:45 pm
chaus писал(а): Из сильных кислот почему-то не обнаружил хлорной. Хотя она часто применяется в лабораторной практике.
Со всеми имеющимися катионами она даёт растворимые соли (даже KClO4 преодолевает порог), поэтому решил не перегружать таблицу (и так всё еле помещается).
SkydiVAR писал(а):
Droog_Andrey писал(а): Я думал добавить звёздочку «разлагается при выделении из раствора»
Как по мне — «плюсадин», как минимум.
Я бы так и сделал сразу, если б было куда впихнуть легенду к звёздочке Впрочем, постараюсь как-нибудь подвинуть, авось втиснется.
2^74207281-1 is prime!
chaus Сообщения: 3135 Зарегистрирован: Вт дек 24, 2013 2:37 pm
Re: Обновил таблицу растворимости
Сообщение chaus » Пн авг 25, 2014 9:10 pm
Droog_Andrey писал(а): (и так всё еле помещается).
Физические константы и кратные/дольные единицы в этой таблице явно чужие. Можно поместить справа легенду и добавить пару-тройку строчек. Как ни крути, хлорная — любимая среда многих координационщиков, спектроскопистов и коррозионистов. Уксусная и лимонная прописались во многих неорганических лабораториях, как дома.
When you open your heart to patriotism, there is no room for prejudice.
Droog_Andrey Сообщения: 2664 Зарегистрирован: Сб сен 29, 2007 8:29 pm Контактная информация:
Re: Обновил таблицу растворимости
Сообщение Droog_Andrey » Пн авг 25, 2014 9:32 pm
chaus писал(а): Физические константы и кратные/дольные единицы в этой таблице явно чужие. Можно поместить справа легенду и добавить пару-тройку строчек
Не, таких кардинальных изменений дизайна не будет
chaus писал(а): Как ни крути, хлорная — любимая среда многих координационщиков, спектроскопистов и коррозионистов.
Ну и хорошо. Школьники-то тут причём? Хватит с них растворимых нитратов
chaus писал(а): Уксусная и лимонная прописались во многих неорганических лабораториях, как дома.
Органику добавлять неохота. Да и формиаты с ацетатами почти все растворимы, а цитраты — вообще глубокая органика, и трудно найти инфу по ним.
Droog_Andrey писал(а): Впрочем, постараюсь как-нибудь подвинуть, авось втиснется.
Звёздочки добавил, картинка по ссылке в первом сообщении снова обновилась!
2^74207281-1 is prime!
Alex K Сообщения: 761 Зарегистрирован: Вт авг 09, 2011 7:29 pm
Re: Обновил таблицу растворимости
Сообщение Alex K » Пн авг 25, 2014 11:25 pm
Собираюсь выпускать в тираж. Может, какие вопросы/уточнения/ошибки заметите — пишите.
Пожалуйста:
1. Если разносите кислоты и основания по слабым-средним-сильным — укажите критерии отнесения (например, достижимость в водном растворе pH такого-то). И хромовая кислота, вроде, таки сильная. И H2SiF6 — тоже.
2. Насколько амфотерен Cu(OH)2 ? Т.е. по факту там сильное преобладание основных свойств, а если уж совсем формально смотреть, то и HNO3 — амфотерный гидроксид с сильным преобладанием кислотных свойств
3. Pb(OH)2 и MgCO3 раньше в таких таблицах относили к нерастворимым.
4. BaF2 — нерастворим.
5. Вы уверены в нерастворимости кучи приведенных Вами цианидов? Несмотря на комплексообразование?
6. Может, строку с ацетатами (традиционную) стоит добавить?
7. Вы уверены в мало (а не «не») растворимости FePO4 ?
8. Хорошо растворим, наверное, таки NH3, а не NH4OH
9. Придирка — Ca3(PO4)2 — разлагается водой (в ТД равновесной системе)
uchebnik fiziki Сообщения: 4265 Зарегистрирован: Пн авг 20, 2012 9:04 pm
Re: Обновил таблицу растворимости
Сообщение uchebnik fiziki » Пн авг 25, 2014 11:44 pm
Droog_Andrey писал(а): Разумеется, гидроксид кальция — щёлочь, а гидроксид аммония — нет. Сила основания не связана с его растворимостью.
То есть NH4OH диссоциирует не нацело? Это новое слово в химической науке, кажется. Может, раствор аммиака в воде и не щёлочь, но гидроксид аммония — однозначно сильное основание.
Хотя сама идея вот этих школьных таблиц с тремя градациями по массовой доле растворённого вещества бесконечно ущербна.
Свобода, равенство, братство.
Droog_Andrey Сообщения: 2664 Зарегистрирован: Сб сен 29, 2007 8:29 pm Контактная информация:
Re: Обновил таблицу растворимости
Сообщение Droog_Andrey » Пн авг 25, 2014 11:46 pm
Alex K писал(а): Пожалуйста:
1. Лично растворял хромат свинца в азотке, а гексафторкремниевая существенно уступает хромовой. Критерий — значение pKa, указывать его не обязательно, кому интересно — выяснит сам, это же учебная таблица
2. Гидроксид меди легко растворяется в не самой крепкой щёлочи. Остальные — увы.
3, 4, 7: У них растворимость превышает 0.01 г / 100 г воды. Свинец удерживается в растворе за счёт образования кластеров вроде [OPb4](PbOH)2(OH)6 2+ . Магний садится при меньшей концентрации из-за образования основных солей, а у среднего карбоната растворимость чуть выше 0.01. У фторида бария 0.16. Фосфат железа в водной среде комплексует и поэтому способен содержаться в количествах, существенно превышающих расчётные через ПР (вообще это часто встречающася ситуация); у него грубые оценки растворимости около 0.02. Не было бы этой растворимости — не встречались бы в природе большие кристаллы штренгита.
5. Цианид, фторсиликат, оксалат, иодат и хромат я добавил недавно, поэтому не по всем катионам данные для них надёжны. У вас есть какие-то источники, которые опровергали бы то, что есть в таблице?
6. Нет, ацетаты я выкинул ещё давно, вместе с формиатами.
8. И ионы аммония, и гидроксид-анионы содержатся в значительных количествах в аммиачной воде. Более того, нет никаких требований по поводу того, в какой форме должно плавать вещество. Сульфид аммония почти полностью плавает в виде NH4HS+NH3. На подобные ситуации указывают звёздочки.
9. Тогда бы фосфорит не встречался в природе
uchebnik fiziki писал(а): То есть NH4OH диссоциирует не нацело?
Конечно, поскольку значительная его часть переходит в молекулярную форму NH3+H2O. Точно по такой же причине, например, PCl4 + PCl6 — является слабым электролитом: в значительной степени переходит в молекулярный PCl5.
А если рассуждать так, как Вы (не учитывать молекулярную форму), то и цианид ртути станет сильным электролитом.
Вообще же говорить о гидроксиде аммония как о самостоятельном соединении нельзя. При низких температурах самостоятельно существует гидрат аммиака, но у него молекулярное строение, а не ионное.
uchebnik fiziki писал(а): Хотя сама идея вот этих школьных таблиц с тремя градациями по массовой доле растворённого вещества бесконечно ущербна.
Это не мешает успешно пользоваться такими таблицами в образовательном процессе
Последний раз редактировалось Droog_Andrey Вт авг 26, 2014 12:22 am, всего редактировалось 1 раз.
2^74207281-1 is prime!
Alex K Сообщения: 761 Зарегистрирован: Вт авг 09, 2011 7:29 pm
Re: Обновил таблицу растворимости
Сообщение Alex K » Вт авг 26, 2014 12:10 am
Droog_Andrey писал(а): 1. Лично растворял хромат свинца в азотке, а гексафторкремниевая существенно уступает хромовой. Критерий — значение pKa, указывать его не обязательно, кому интересно — выяснит сам, это же учебная таблица
2. Гидроксид меди легко растворяется в не самой крепкой щёлочи. Остальные — увы.
3, 4, 7: У них растворимость превышает 0.01 г / 100 г воды. Магний садится при меньшей концентрации из-за образования основных солей, а у среднего карбоната растворимость чуть выше 0.01. У фторида бария 0.16. Фосфат железа в водной среде комплексует и поэтому способен содержаться в количествах, существенно превышающих расчётные через ПР (вообще это часто встречающася ситуация); у него грубые оценки растворимости около 0.02. Не было бы этой растворимости — не встречались бы в природе большие кристаллы штренгита.
5. Цианид, фторсиликат, оксалат, иодат и хромат я добавил недавно, поэтому не по всем катионам данные для них надёжны. У вас есть какие-то источники, которые опровергали бы то, что есть в таблице?
6. Нет, ацетаты я выкинул ещё давно, вместе с формиатами.
8. И ионы аммония, и гидроксид-анионы содержатся в значительных количествах в аммиачной воде. Более того, нет никаких требований по поводу того, в какой форме должно плавать вещество. Сульфид аммония почти полностью плавает в виде NH4HS+NH3. На подобные ситуации указывают звёздочки.
9. Тогда бы фосфорит не встречался в природе
1. Не показатель. В кислой среде хромат-ион димеризуется (и это в школьной программе есть). pK будут не очень хорошо работать для оснований (а ПР описывает уже гетерогенное равновесие), так что по достижимому pH, ИМХО, лучше.
2. А не при кипячении в концентрированной (щелочи)? В стандартной реакции на те же альдегиды никуда он не растворяется.
3,4,7 — завтра на работе по справочнику гляну (по памяти BaF2 растворим весьма слабо, но он тяжелый. ). По фосфату железа 3 — возможно, но тогда то же будет и для цианидов? А большие кристаллы растут в природе в гидротерме и долго, а потому для это достаточен и не слишком быстрый массоперенос
8. А тут появляется вопрос о степени диссоциации именно ионного NH4OH (которая таки 100%)
9. А вы проверьте по константам Фосфорит (который из гуано) — это плохо закристаллизованный апатит, Ca3(PO4)2 — это витлокит — метаморфическая штука
Droog_Andrey Сообщения: 2664 Зарегистрирован: Сб сен 29, 2007 8:29 pm Контактная информация:
Re: Обновил таблицу растворимости
Сообщение Droog_Andrey » Вт авг 26, 2014 12:35 am
1. Меряться pH хромовая не осилит, ибо перейдёт в двухромовую. Всё же вытеснение — показатель: сильные кислоты друг друга не вытесняют так, чтобы осадки растворялись. Да и не переходила бы она в дихромовую, если бы была посильней. Вон сульфит натрия в Na2S2O5 точно так же переходит. А гидросульфат в пиросульфат в растворе не переведёшь. Так что хромовая таки недостаточно сильна. Для оснований тоже можно использовать вытеснение (гидроксид магния вытесняет аммиак из солей аммония). В целом и кислоты, и основания упорядочены примерно по убыванию силы.
2. Нет. Кипячение в двадцатимолярной щёлочи нужно для закомплексовывания железа(II) и магния, причём воспроизводятся эти методики плохо. А синтез гидроксокупратов — студенческий практикум. Кстати, шиш бы пошла стандартная реакция на альдегиды без повышенной растворимости меди(II) в щёлочи.
3. Цианид железа(III) сам по себе не получается. В избытке цианида получается комплекс, а если добиваться осаждения, то получаются либо основные, либо двойные соли. Железо(II) гидролизует меньше, и его удаётся осадить. Получается полимерная штука, как и с никелем и т.п.
По поводу справочника повеселили. Я при составлении таблицы смотрел в дюжине справочников и проверял источники, на которые эти справочники ссылаются, просматривал монографии и гуглил конкретные статьи по веществам. Если бы я ограничился одним справочником — то получилась бы просто ещё одна таблица с кучей ошибок.
8. Так можно взять любой электролит и рассмотреть именно ионную его часть, и степень диссоциации всегда будет 100% Возьмите гидроксид оксония — и вот вам и щёлочь, и сильная кислота одновременно
9. Да фиг с ними, с константами. На практике средний фосфат кальция нерастворим и спокойно лежит в водной среде. Может, за сто лет он и развалится на Ca5(PO4)3OH + CaHPO4, но с таким подходом надо чуть ли не половину веществ объявлять неустойчивыми. Термодинамически нам всем вообще выгодно стать большой железной болванкой.
2^74207281-1 is prime!
Alex K Сообщения: 761 Зарегистрирован: Вт авг 09, 2011 7:29 pm
Re: Обновил таблицу растворимости
Сообщение Alex K » Вт авг 26, 2014 1:57 pm
Droog_Andrey писал(а): 1. Меряться pH хромовая не осилит, ибо перейдёт в двухромовую. Всё же вытеснение — показатель: сильные кислоты друг друга не вытесняют так, чтобы осадки растворялись. Да и не переходила бы она в дихромовую, если бы была посильней. Вон сульфит натрия в Na2S2O5 точно так же переходит. А гидросульфат в пиросульфат в растворе не переведёшь. Так что хромовая таки недостаточно сильна. Для оснований тоже можно использовать вытеснение (гидроксид магния вытесняет аммиак из солей аммония). В целом и кислоты, и основания упорядочены примерно по убыванию силы.
2. Нет. Кипячение в двадцатимолярной щёлочи нужно для закомплексовывания железа(II) и магния, причём воспроизводятся эти методики плохо. А синтез гидроксокупратов — студенческий практикум. Кстати, шиш бы пошла стандартная реакция на альдегиды без повышенной растворимости меди(II) в щёлочи.
3. Цианид железа(III) сам по себе не получается. В избытке цианида получается комплекс, а если добиваться осаждения, то получаются либо основные, либо двойные соли. Железо(II) гидролизует меньше, и его удаётся осадить. Получается полимерная штука, как и с никелем и т.п.
По поводу справочника повеселили. Я при составлении таблицы смотрел в дюжине справочников и проверял источники, на которые эти справочники ссылаются, просматривал монографии и гуглил конкретные статьи по веществам. Если бы я ограничился одним справочником — то получилась бы просто ещё одна таблица с кучей ошибок.
8. Так можно взять любой электролит и рассмотреть именно ионную его часть, и степень диссоциации всегда будет 100% Возьмите гидроксид оксония — и вот вам и щёлочь, и сильная кислота одновременно
9. Да фиг с ними, с константами. На практике средний фосфат кальция нерастворим и спокойно лежит в водной среде. Может, за сто лет он и развалится на Ca5(PO4)3OH + CaHPO4, но с таким подходом надо чуть ли не половину веществ объявлять неустойчивыми. Термодинамически нам всем вообще выгодно стать большой железной болванкой.
Берем Лурье (справочник по аналитической химии)
1. Для H2CrO4 pKa=0.8. И где у Вас граница «сильная-слабая» тогда? Более того, H2Cr2O7 по первой ступени диссоциирует полностью, а Вы сами писали, что конкретная форма нахождения в растворе Вас не очень волнует. Кроме того, есть правило, что кислоты (OH)nЭOm с m>1 — сильные.
2. Из того источника. pH осаждения гидроксидов — начало растворения (неколичественность осаждения) Cu(OH)2 — 14. Как и у Fe(OH)3, кстати. НО: у Fe(OH)2 и Ni(OH)2 этот pH ниже! Для полного растворения Cu(OH)2 нужна 40-50% NaOH (справочник Лидин. Молочко, Андреева) , Турова в таблицах указывает просто «конц».
3. Ну, а я о чем?
9. На самом деле, не 100 лет, а дней 10. И этот момент, кстати, используют при разработке биорезорбируемых костных имплантов.
Таблица растворимости солей, кислот и оснований
Таблица растворимости вместе с таблицей Менделеева являются основным теоретическим материалом при изучении химии! Растворимость — способность вещества образовывать с другими веществами однородные системы — растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц.
Если при изучении материала на данной странице у Вас возникнут вопросы, Вы всегда можете задать их на нашем форуме. Также на Вам помогут решить задачи по химии, теории вероятности, математике, геометрии и многим другим предметам!
Полная таблица растворимости солей, кислот и оснований
Условные обозначения таблицы растворимости:
Р — вещество хорошо растворимо в воде;
М — вещество малорастворимо в воде;
Н — вещество практически нерастворимо в воде, но легко растворяется в слабых или разбавленных кислотах;
РК — вещество нерастворимо в воде и растворяется только в сильных неорганических кислотах;
НК — вещество нерастворимо ни в воде, ни в кислотах;
Г — вещество полностью гидролизуется при растворении и не существует в контакте с водой;
— — вещество не существует.
Стандартная (школьная) таблица растворимости
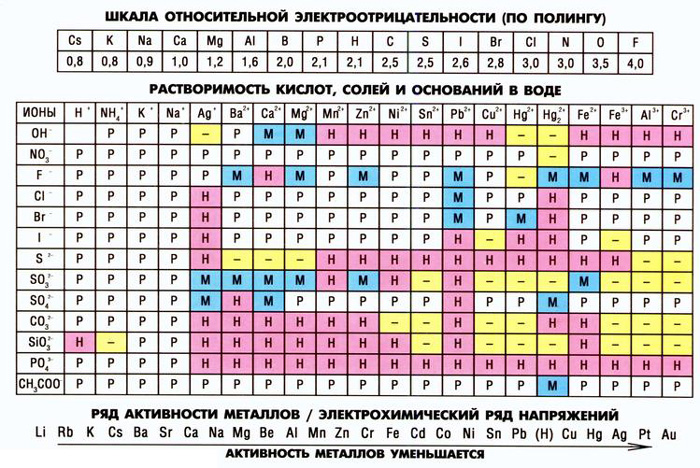
Таблица растворимости используют для проверки условий протекания реакции, так как одним из условий протекания реакции является образование осадка (необратимость протекания реакции), то по таблице расворимости можно проверить образование осадка и тем самым определить, протекает реакиция или нет.
Помимо таблицы растворимости на сайте Вы можете посмотреть тригонометрические формулы, таблицу производных и таблицу интегралов. Пользуйтесь на здоровье!